Novel Genetic and Molecular Regulation of HDL Metabolism
Total Page:16
File Type:pdf, Size:1020Kb

Load more
Recommended publications
-

Silencing of Phosphoinositide-Specific
ANTICANCER RESEARCH 34: 4069-4076 (2014) Silencing of Phosphoinositide-specific Phospholipase C ε Remodulates the Expression of the Phosphoinositide Signal Transduction Pathway in Human Osteosarcoma Cell Lines VINCENZA RITA LO VASCO1, MARTINA LEOPIZZI2, DANIELA STOPPOLONI3 and CARLO DELLA ROCCA2 Departments of 1Sense Organs , 2Medicine and Surgery Sciences and Biotechnologies and 3Biochemistry Sciences “A. Rossi Fanelli”, Sapienza University, Rome, Italy Abstract. Background: Ezrin, a member of the signal transduction pathway (5). The reduction of PIP2 ezrin–radixin–moesin family, is involved in the metastatic induces ezrin dissociation from the plasma membrane (6). spread of osteosarcoma. Ezrin binds phosphatydil inositol-4,5- The levels of PIP2 are regulated by the PI-specific bisphosphate (PIP2), a crucial molecule of the phospholipase C (PI-PLC) family (7), constituting thirteen phosphoinositide signal transduction pathway. PIP2 levels are enzymes divided into six sub-families on the basis of amino regulated by phosphoinositide-specific phospholipase C (PI- acid sequence, domain structure, mechanism of recruitment PLC) enzymes. PI-PLCε isoform, a well-characterized direct and tissue distribution (7-15). PI-PLCε, a direct effector of effector of rat sarcoma (RAS), is at a unique convergence RAS (14-15), might be the point of convergence for the point for the broad range of signaling pathways that promote broad range of signalling pathways that promote the RAS GTPase-mediated signalling. Materials and Methods. By RASGTPase-mediated signalling (16). using molecular biology methods and microscopic analyses, In previous studies, we suggested a relationship between we analyzed the expression of ezrin and PLC genes after PI-PLC expression and ezrin (17-18). -

The Role of Genetic Variation in Predisposition to Alcohol-Related Chronic Pancreatitis
The Role of Genetic Variation in Predisposition to Alcohol-related Chronic Pancreatitis Thesis submitted in accordance with the requirements of the University of Liverpool for the degree of Doctor in Philosophy by Marianne Lucy Johnstone April 2015 The Role of Genetic Variation in Predisposition to Alcohol-related Chronic Pancreatitis 2015 Abstract Background Chronic pancreatitis (CP) is a disease of fibrosis of the pancreas for which alcohol is the main causative agent. However, only a small proportion of alcoholics develop chronic pancreatitis. Genetic polymorphism may affect pancreatitis risk. Aim To determine the factors required to classify a chronic pancreatic population and identify genetic variations that may explain why only some alcoholics develop chronic pancreatitis. Methods The most appropriate method of diagnosing CP was assessed using a systematic review. Genetics of different populations of alcohol-related chronic pancreatitics (ACP) were explored using four different techniques: genome-wide association study (GWAS); custom arrays; PCR of variable nucleotide tandem repeats (VNTR) and next generation sequencing (NGS) of selected genes. Results EUS and sMR were identified as giving the overall best sensitivity and specificity for diagnosing CP. GWAS revealed two associations with CP (identified and replicated) at PRSS1-PRSS2_rs10273639 (OR 0.73, 95% CI 0.68-0.79) and X-linked CLDN2_rs12688220 (OR 1.39, 1.28-1.49) and the association was more pronounced in the ACP group (OR 0.56, 0.48-0.64)and OR 2.11, 1.84-2.42). The previously identified VNTR in CEL was shown to have a lower frequency of the normal repeat in ACP than alcoholic liver disease (ALD; OR 0.61, 0.41-0.93). -

Genetic Variants in PLCB4/PLCB1 As Susceptibility Loci for Coronary Artery
www.nature.com/scientificreports OPEN Genetic variants in PLCB4/PLCB1 as susceptibility loci for coronary artery aneurysm formation in Received: 27 March 2015 Accepted: 04 September 2015 Kawasaki disease in Han Chinese Published: 05 October 2015 in Taiwan Ying-Ju Lin1,2, Jeng-Sheng Chang3,4, Xiang Liu5, Hsinyi Tsang5, Wen-Kuei Chien6, Jin-Hua Chen6,7, Hsin-Yang Hsieh3,8, Kai-Chung Hsueh9, Yi-Tzone Shiao10, Ju-Pi Li2,11, Cheng-Wen Lin12, Chih-Ho Lai13, Jer-Yuarn Wu2,14, Chien-Hsiun Chen2,14, Jaung-Geng Lin2, Ting-Hsu Lin1, Chiu-Chu Liao1, Shao-Mei Huang1, Yu-Ching Lan15, Tsung-Jung Ho2, Wen-Miin Liang16, Yi-Chun Yeh16, Jung-Chun Lin17 & Fuu-Jen Tsai1,2,18 Kawasaki disease (KD) is an acute, inflammatory, and self-limited vasculitis affecting infants and young children. Coronary artery aneurysm (CAA) formation is the major complication of KD and the leading cause of acquired cardiovascular disease among children. To identify susceptible loci that might predispose patients with KD to CAA formation, a genome-wide association screen was performed in a Taiwanese KD cohort. Patients with both KD and CAA had longer fever duration and delayed intravenous immunoglobulin treatment time. After adjusting for these factors, 100 susceptibility loci were identified. Four genes were identified from a single cluster of 35 using the Ingenuity Pathway Analysis (IPA) Knowledge Base. Silencing KCNQ5, PLCB1, PLCB4, and PLCL1 inhibited the effect of lipopolysaccharide-induced endothelial cell inflammation with varying degrees of proinflammatory cytokine expression. PLCB1 showed the most significant inhibition. Endothelial cell inflammation was also inhibited by using a phospholipase C (PLC) inhibitor. -

Regulation of Signaling and Metabolism by Lipin-Mediated Phosphatidic Acid Phosphohydrolase Activity
biomolecules Review Regulation of Signaling and Metabolism by Lipin-mediated Phosphatidic Acid Phosphohydrolase Activity Andrew J. Lutkewitte and Brian N. Finck * Center for Human Nutrition, Division of Geriatrics and Nutritional Sciences, Department of Medicine, Washington University School of Medicine, Euclid Avenue, Campus Box 8031, St. Louis, MO 63110, USA; [email protected] * Correspondence: bfi[email protected]; Tel: +1-3143628963 Received: 4 September 2020; Accepted: 24 September 2020; Published: 29 September 2020 Abstract: Phosphatidic acid (PA) is a glycerophospholipid intermediate in the triglyceride synthesis pathway that has incredibly important structural functions as a component of cell membranes and dynamic effects on intracellular and intercellular signaling pathways. Although there are many pathways to synthesize and degrade PA, a family of PA phosphohydrolases (lipin family proteins) that generate diacylglycerol constitute the primary pathway for PA incorporation into triglycerides. Previously, it was believed that the pool of PA used to synthesize triglyceride was distinct, compartmentalized, and did not widely intersect with signaling pathways. However, we now know that modulating the activity of lipin 1 has profound effects on signaling in a variety of cell types. Indeed, in most tissues except adipose tissue, lipin-mediated PA phosphohydrolase activity is far from limiting for normal rates of triglyceride synthesis, but rather impacts critical signaling cascades that control cellular homeostasis. In this review, we will discuss how lipin-mediated control of PA concentrations regulates metabolism and signaling in mammalian organisms. Keywords: phosphatidic acid; diacylglycerol; lipin; signaling 1. Introduction Foundational work many decades ago by the laboratory of Dr. Eugene Kennedy defined the four sequential enzymatic steps by which three fatty acyl groups were esterified onto the glycerol-3-phosphate backbone to synthesize triglyceride [1]. -

The Metabolic Serine Hydrolases and Their Functions in Mammalian Physiology and Disease Jonathan Z
REVIEW pubs.acs.org/CR The Metabolic Serine Hydrolases and Their Functions in Mammalian Physiology and Disease Jonathan Z. Long* and Benjamin F. Cravatt* The Skaggs Institute for Chemical Biology and Department of Chemical Physiology, The Scripps Research Institute, 10550 North Torrey Pines Road, La Jolla, California 92037, United States CONTENTS 2.4. Other Phospholipases 6034 1. Introduction 6023 2.4.1. LIPG (Endothelial Lipase) 6034 2. Small-Molecule Hydrolases 6023 2.4.2. PLA1A (Phosphatidylserine-Specific 2.1. Intracellular Neutral Lipases 6023 PLA1) 6035 2.1.1. LIPE (Hormone-Sensitive Lipase) 6024 2.4.3. LIPH and LIPI (Phosphatidic Acid-Specific 2.1.2. PNPLA2 (Adipose Triglyceride Lipase) 6024 PLA1R and β) 6035 2.1.3. MGLL (Monoacylglycerol Lipase) 6025 2.4.4. PLB1 (Phospholipase B) 6035 2.1.4. DAGLA and DAGLB (Diacylglycerol Lipase 2.4.5. DDHD1 and DDHD2 (DDHD Domain R and β) 6026 Containing 1 and 2) 6035 2.1.5. CES3 (Carboxylesterase 3) 6026 2.4.6. ABHD4 (Alpha/Beta Hydrolase Domain 2.1.6. AADACL1 (Arylacetamide Deacetylase-like 1) 6026 Containing 4) 6036 2.1.7. ABHD6 (Alpha/Beta Hydrolase Domain 2.5. Small-Molecule Amidases 6036 Containing 6) 6027 2.5.1. FAAH and FAAH2 (Fatty Acid Amide 2.1.8. ABHD12 (Alpha/Beta Hydrolase Domain Hydrolase and FAAH2) 6036 Containing 12) 6027 2.5.2. AFMID (Arylformamidase) 6037 2.2. Extracellular Neutral Lipases 6027 2.6. Acyl-CoA Hydrolases 6037 2.2.1. PNLIP (Pancreatic Lipase) 6028 2.6.1. FASN (Fatty Acid Synthase) 6037 2.2.2. PNLIPRP1 and PNLIPR2 (Pancreatic 2.6.2. -

A Meta-Analysis of Gene Expression Data Highlights Synaptic Dysfunction
www.nature.com/scientificreports OPEN A meta-analysis of gene expression data highlights synaptic dysfunction in the hippocampus of brains with Alzheimer’s disease Saeedeh Hosseinian1, Ehsan Arefan2,3 ✉ , Hassan Rakhsh-Khorshid4, Mehdi Eivani 5, Ameneh Rezayof6, Hamid Pezeshk 7,8 & Sayed-Amir Marashi 1 Since the world population is ageing, dementia is going to be a growing concern. Alzheimer’s disease is the most common form of dementia. The pathogenesis of Alzheimer’s disease is extensively studied, yet unknown remains. Therefore, we aimed to extract new knowledge from existing data. We analysed about 2700 upregulated genes and 2200 downregulated genes from three studies on the CA1 of the hippocampus of brains with Alzheimer’s disease. We found that only the calcium signalling pathway enriched by 48 downregulated genes was consistent between all three studies. We predicted miR-129 to target nine out of 48 genes. Then, we validated miR-129 to regulate six out of nine genes in HEK cells. We noticed that four out of six genes play a role in synaptic plasticity. Finally, we confrmed the upregulation of miR-129 in the hippocampus of brains of rats with scopolamine-induced amnesia as a model of Alzheimer’s disease. We suggest that future research should investigate the possible role of miR-129 in synaptic plasticity and Alzheimer’s disease. This paper presents a novel framework to gain insight into potential biomarkers and targets for diagnosis and treatment of diseases. Alzheimer’s disease (AD) is the most common form of dementia. It mostly afects people aged 65 and older, pro- gresses slowly and leads to death in an average of nine years afer diagnosis. -

Overexpression of Hormone-Sensitive Lipase Prevents Triglyceride Accumulation in Adipocytes
Overexpression of hormone-sensitive lipase prevents triglyceride accumulation in adipocytes. C Sztalryd, … , M C Komaromy, F B Kraemer J Clin Invest. 1995;95(6):2652-2661. https://doi.org/10.1172/JCI117967. Research Article Hormone-sensitive lipase (HSL) is a cytosolic neutral lipase that hydrolyzes intracellular stores of triglycerides within adipocytes and is thought to be the rate limiting enzyme in lipolysis; however, direct evidence to prove this concept has been lacking. The present study was designed to establish the function of HSL in adipocytes. A 2360-bp fragment containing the entire HSL coding region was cloned into the vector pCEP4 and was used to transfect the 3T3-F442A adipogenic cell line. Nondifferentiated, transfected cells were screened for HSL overexpression by indirect immunofluorescence microscopy and confirmed by immunoblotting cell extracts with anti-HSL/fusion protein antibodies and by Northern blots for HSL mRNA. Stable transfectants overexpressing HSL were obtained and cloned. Compared with undifferentiated 3T3-F442A cells transfected with pCEP4 not containing the insert (vector alone) where HSL expression was very low, undifferentiated HSL transfectants had up to a 100-fold increase in HSL activity. Likewise, immunoreactive HSL protein and HSL mRNA levels were increased up to 100-fold in HSL transfectants. When confluent cells were allowed to differentiate by exposure to insulin, HSL expression increased in vector alone transfected cells, but remained below that observed in HSL transfectants. A similar degree of differentiation was seen in both vector alone and HSL transfectants when based on the induction of lipoprotein lipase. Cellular triglyceride content increased dramatically in the vector alone transfected cells […] Find the latest version: https://jci.me/117967/pdf Overexpression of Hormone-sensitive Lipase Prevents Triglyceride Accumulation in Adipocytes Carole Sztalryd, Michael C. -
Supplementary Data
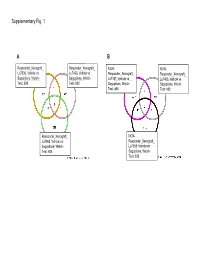
Supplementary Fig. 1 A B Responder_Xenograft_ Responder_Xenograft_ NON- NON- Lu7336, Vehicle vs Lu7466, Vehicle vs Responder_Xenograft_ Responder_Xenograft_ Sagopilone, Welch- Sagopilone, Welch- Lu7187, Vehicle vs Lu7406, Vehicle vs Test: 638 Test: 600 Sagopilone, Welch- Sagopilone, Welch- Test: 468 Test: 482 Responder_Xenograft_ NON- Lu7860, Vehicle vs Responder_Xenograft_ Sagopilone, Welch - Lu7558, Vehicle vs Test: 605 Sagopilone, Welch- Test: 333 Supplementary Fig. 2 Supplementary Fig. 3 Supplementary Figure S1. Venn diagrams comparing probe sets regulated by Sagopilone treatment (10mg/kg for 24h) between individual models (Welsh Test ellipse p-value<0.001 or 5-fold change). A Sagopilone responder models, B Sagopilone non-responder models. Supplementary Figure S2. Pathway analysis of genes regulated by Sagopilone treatment in responder xenograft models 24h after Sagopilone treatment by GeneGo Metacore; the most significant pathway map representing cell cycle/spindle assembly and chromosome separation is shown, genes upregulated by Sagopilone treatment are marked with red thermometers. Supplementary Figure S3. GeneGo Metacore pathway analysis of genes differentially expressed between Sagopilone Responder and Non-Responder models displaying –log(p-Values) of most significant pathway maps. Supplementary Tables Supplementary Table 1. Response and activity in 22 non-small-cell lung cancer (NSCLC) xenograft models after treatment with Sagopilone and other cytotoxic agents commonly used in the management of NSCLC Tumor Model Response type -

Supplementary Materials and Tables a and B
SUPPLEMENTARY MATERIAL 1 Table A. Main characteristics of the subset of 23 AML patients studied by high-density arrays (subset A) WBC BM blasts MYST3- MLL Age/Gender WHO / FAB subtype Karyotype FLT3-ITD NPM status (x109/L) (%) CREBBP status 1 51 / F M4 NA 21 78 + - G A 2 28 / M M4 t(8;16)(p11;p13) 8 92 + - G G 3 53 / F M4 t(8;16)(p11;p13) 27 96 + NA G NA 4 24 / M PML-RARα / M3 t(15;17) 5 90 - - G G 5 52 / M PML-RARα / M3 t(15;17) 1.5 75 - - G G 6 31 / F PML-RARα / M3 t(15;17) 3.2 89 - - G G 7 23 / M RUNX1-RUNX1T1 / M2 t(8;21) 38 34 - + ND G 8 52 / M RUNX1-RUNX1T1 / M2 t(8;21) 8 68 - - ND G 9 40 / M RUNX1-RUNX1T1 / M2 t(8;21) 5.1 54 - - ND G 10 63 / M CBFβ-MYH11 / M4 inv(16) 297 80 - - ND G 11 63 / M CBFβ-MYH11 / M4 inv(16) 7 74 - - ND G 12 59 / M CBFβ-MYH11 / M0 t(16;16) 108 94 - - ND G 13 41 / F MLLT3-MLL / M5 t(9;11) 51 90 - + G R 14 38 / F M5 46, XX 36 79 - + G G 15 76 / M M4 46 XY, der(10) 21 90 - - G NA 16 59 / M M4 NA 29 59 - - M G 17 26 / M M5 46, XY 295 92 - + G G 18 62 / F M5 NA 67 88 - + M A 19 47 / F M5 del(11q23) 17 78 - + M G 20 50 / F M5 46, XX 61 59 - + M G 21 28 / F M5 46, XX 132 90 - + G G 22 30 / F AML-MD / M5 46, XX 6 79 - + M G 23 64 / M AML-MD / M1 46, XY 17 83 - + M G WBC: white blood cell. -
Supplementary Table 1
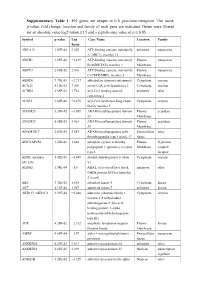
Supplementary Table 1. 492 genes are unique to 0 h post-heat timepoint. The name, p-value, fold change, location and family of each gene are indicated. Genes were filtered for an absolute value log2 ration 1.5 and a significance value of p ≤ 0.05. Symbol p-value Log Gene Name Location Family Ratio ABCA13 1.87E-02 3.292 ATP-binding cassette, sub-family unknown transporter A (ABC1), member 13 ABCB1 1.93E-02 −1.819 ATP-binding cassette, sub-family Plasma transporter B (MDR/TAP), member 1 Membrane ABCC3 2.83E-02 2.016 ATP-binding cassette, sub-family Plasma transporter C (CFTR/MRP), member 3 Membrane ABHD6 7.79E-03 −2.717 abhydrolase domain containing 6 Cytoplasm enzyme ACAT1 4.10E-02 3.009 acetyl-CoA acetyltransferase 1 Cytoplasm enzyme ACBD4 2.66E-03 1.722 acyl-CoA binding domain unknown other containing 4 ACSL5 1.86E-02 −2.876 acyl-CoA synthetase long-chain Cytoplasm enzyme family member 5 ADAM23 3.33E-02 −3.008 ADAM metallopeptidase domain Plasma peptidase 23 Membrane ADAM29 5.58E-03 3.463 ADAM metallopeptidase domain Plasma peptidase 29 Membrane ADAMTS17 2.67E-04 3.051 ADAM metallopeptidase with Extracellular other thrombospondin type 1 motif, 17 Space ADCYAP1R1 1.20E-02 1.848 adenylate cyclase activating Plasma G-protein polypeptide 1 (pituitary) receptor Membrane coupled type I receptor ADH6 (includes 4.02E-02 −1.845 alcohol dehydrogenase 6 (class Cytoplasm enzyme EG:130) V) AHSA2 1.54E-04 −1.6 AHA1, activator of heat shock unknown other 90kDa protein ATPase homolog 2 (yeast) AK5 3.32E-02 1.658 adenylate kinase 5 Cytoplasm kinase AK7 -

Aprioritized Panel of Candidate Genes
In: Advances in Genetics Research. Volume 9 ISBN: 978-1- 62081-466-6 Editor: Kevin V. Urbano © 2012 Nova Science Publishers, Inc No part of this digital document may be reproduced, stored in a retrieval system or transmitted commercially in any form or by any means. The publisher has taken reasonable care in the preparation of this digital document, but makes no expressed or implied warranty of any kind and assumes no responsibility for any errors or omissions. No liability is assumed for incidental or consequential damages in connection with or arising out of information contained herein. This digital document is sold with the clear understanding that the publisher is not engaged in rendering legal, medical or any other professional services. Chapter 1 A PRIORITIZED PANEL OF CANDIDATE GENES TO BE EXPLORED FOR ASSOCIATIONS WITH THE BLOOD PRESSURE RESPONSE TO EXERCISE Garrett I. Ash,1,Amanda L. Augeri,2John D. Eicher,3 Michael L. Bruneau, Jr.1 and Linda S. Pescatello1 1University of Connecticut, Storrs, CT, US 2Hartford Hospital, Hartford, CT, US 3Yale University School of Medicine, New Haven, CT, US ABSTRACT Introduction. Identifying genetic variants associated with the blood pressure (BP) response to exercise is hindered by the lack of standard criteria for candidate gene selection, underpowered samples, and a limited number of conclusive whole genome studies. We developed a prioritized panel of candidate genetic variants that may increase the likelihood of finding genotype associations with the BP response to exercise when used alone or in conjunction with high throughput genotyping studies. Methods. We searched for candidate genetic variants meeting preestablished criteria using PubMed and published systematic reviews. -

Pancreatic Carboxyl Ester Lipase: a Circulating Enzyme That Modifies Normal and Oxidized Lipoproteins in Vitro
Pancreatic carboxyl ester lipase: a circulating enzyme that modifies normal and oxidized lipoproteins in vitro. R Shamir, … , D W Morel, E A Fisher J Clin Invest. 1996;97(7):1696-1704. https://doi.org/10.1172/JCI118596. Research Article Pancreatic carboxyl ester lipase (CEL) hydrolyzes cholesteryl esters (CE), triglycerides (TG), and lysophospholipids, with CE and TG hydrolysis stimulated by cholate. Originally thought to be confined to the gastrointestinal system, CEL has been reported in the plasma of humans and other mammals, implying its potential in vivo to modify lipids associated with LDL, HDL (CE, TG), and oxidized LDL (lysophosphatidylcholine, lysoPC). We measured the concentration of CEL in human plasma as 1.2+/-0.5 ng/ml (in the range reported for lipoprotein lipase). Human LDL and HDL3 reconstituted with radiolabeled lipids were incubated with purified porcine CEL without or with cholate (10 or 100 microM, concentrations achievable in systemic or portal plasma, respectively). Using a saturating concentration of lipoprotein-associated CE (4 microM), with increasing cholate concentration there was an increase in the hydrolysis of LDL- and HDL3-CE; at 100 microM cholate, the present hydrolysis per hour was 32+/-2 and 1.6+/-0.1, respectively, indicating that CEL interaction varied with lipoprotein class. HDL3-TG hydrolysis was also observed, but was only approximately 5-10% of that for HDL3-CE at either 10 or 100 microM cholate. Oxidized LDL (OxLDL) is enriched with lysoPC, a proatherogenic compound. After a 4-h incubation with CEL, the lysoPC content of OxLDL was depleted 57%. Colocalization of CEL in the vicinity of OxLDL formation was supported by demonstrating in human aortic homogenate a cholate-stimulated […] Find the latest version: https://jci.me/118596/pdf Pancreatic Carboxyl Ester Lipase: A Circulating Enzyme That Modifies Normal and Oxidized Lipoproteins In Vitro Raanan Shamir,*‡ William J.