Workshop Salma-Kaouther (1) -.:: ECOPLANTMED
Total Page:16
File Type:pdf, Size:1020Kb
Load more
Recommended publications
-

Diptera: Ceratopogonidae) in Tunisia, with Emphasis on the Bluetongue Vector Culicoides Imicola Hammami S.*, Bouzid M.*, Hammou F.*, Fakhfakh E.* & Delecolle J.C.**
Article available at http://www.parasite-journal.org or http://dx.doi.org/10.1051/parasite/2008152179 OCCURRENCE OF CULICOIDES SPP. (DIPTERA: CERATOPOGONIDAE) IN TUNISIA, WITH EMPHASIS ON THE BLUETONGUE VECTOR CULICOIDES IMICOLA HAMMAMI S.*, BOUZID M.*, HAMMOU F.*, FAKHFAKH E.* & DELECOLLE J.C.** Summary: Résumé : PRÉSENCE DE DIFFÉRENTES ESPÈCES DE CULICOIDES (DIPTERA : CERATOPOGONIDAE) EN TUNISIE, EN PARTICULIER DE Following the bluetongue (BT) outbreaks in Tunisia from 1999 to CULICOIDES IMICOLA, VECTEUR DE LA FIÈVRE CATARRHALE OVINE 2002, BTV (bluetongue virus) serotype 2 was isolated; however, no entomological investigation was performed. In the study Suite à l’incursion de la fièvre catarrhale ovine (bluetongue) en presented here, we assessed the Culicoides species populations Tunisie en 1999, le sérotype 2 du virus responsable a été isolé, (particularly C. imicola) in proximity to the BT outbreaks locations, toutefois, aucune investigation entomologique n’a été entreprise. both as a retrospective analysis and to update the list of Dans cette étude, nous avons évalué les populations de Culicoides Culicoides species present in Tunisia. The insects were caught (en particulier C. imicola) à proximité des foyers de la maladie, using light traps and the species identification was performed comme approche rétrospective et pour mettre à jour la liste des according to the standard entomological methods. This study espèces de Culicoides présentes dans le pays. Les insectes ont été revealed the presence of significant numbers of C. imicola in all capturés en utilisant des pièges lumineux. Cette étude a permis de the tested locations. In addition, we reported a new Culicoides détecter un grand nombre de C. -

Par Décret N° 2013-3721 Du 2 Septembre 2013. Art
Par décret n° 2013-3721 du 2 septembre 2013. Art. 2 - Est abrogé, l'arrêté du ministre de Monsieur Jalel Daoues, technicien en chef, est l'agriculture et des ressources hydrauliques du 12 mars chargé des fonctions de chef de service à 2008, portant approbation du plan directeur des l’arrondissement de la protection des eaux et des sols centres de collecte et de transport du lait frais. au commissariat régional au développement agricole Art. 3 - Le présent arrêté sera publié au Journal de Sousse. Officiel de la République Tunisienne. Tunis, le 2 août 2013. Par décret n° 2013-3722 du 2 septembre 2013. Le ministre de l'agriculture Monsieur Naceur Chériak, ingénieur des travaux, Mohamed Ben Salem est chargé des fonctions de chef de la cellule Vu territoriale de vulgarisation agricole « Menzel El Le Chef du Gouvernement Habib » au commissariat régional au développement Ali Larayedh agricole de Gabès. Plan directeur des centres de collecte et de transport du Arrêté du ministre de l'agriculture du 2 août lait frais 2013, portant approbation du plan directeur Article premier – Les centres de collecte et de des centres de collecte et de transport du lait transport du lait frais sont créés conformément au frais. cahier des charges approuvé par l'arrêté du 23 juin Le ministre de l'agriculture, 2011 susvisé et au présent plan directeur. Vu la loi constituante n° 2011-6 du 16 décembre Art. 2 - Le plan directeur fixe la répartition 2011, portant organisation provisoire des pouvoirs géographique des centres de collecte et de transport du publics, lait frais pour chaque gouvernorat selon les critères suivants : Vu la loi n° 2005-95 du 18 octobre 2005, relative à - l'évolution du cheptel des bovins laitiers. -

Quelques Aspects Problematiques Dans La Transcription Des Toponymes Tunisiens
QUELQUES ASPECTS PROBLEMATIQUES DANS LA TRANSCRIPTION DES TOPONYMES TUNISIENS Mohsen DHIEB Professeur de géographie (cartographie) Laboratoire SYFACTE FLSH de Sfax TUNISIE [email protected] Introduction Quelle que soit le pays ou la langue d’usage, la transcription toponymique des noms de lieux géographiques sur un atlas ou un autre document cartographique en particulier ou tout autre document d’une façon générale pose problème notamment dans des pays où il n’y a pas de tradition ou de « politique » toponymique. Il en est de même pour les contrées « ouvertes » à l’extérieur et par conséquent ayant subi ou subissant encore les influences linguistiques étrangères ou alors dans des régions caractérisées par la complexité de leur situation linguistique. C’est particulièrement le cas de la Tunisie, pays méditerranéen bien « ancré » dans l’histoire, mais aussi bien ouvert à l’étranger et subissant les soubresauts de la mondialisation, et manquant par ailleurs cruellement de politique toponymique. Tout ceci malgré l’intérêt que certains acteurs aux profils différents y prêtent depuis peu, intérêt matérialisé, entre autres manifestations scientifiques, par l’organisation de deux rencontres scientifiques par la Commission du GENUING en 2005 et d’une autre août 2008 à Tunis, lors du 35ème Congrès de l’UGI. Aussi, il s’agit dans le cadre de cette présentation générale de la situation de la transcription toponymique en Tunisie, dans un premier temps, de dresser l’état des lieux, de mettre en valeur les principales difficultés rencontrées en manipulant les noms géographiques dans leurs différentes transcriptions dans un second temps. En troisième lieu, il s’agit de proposer à l’officialisation, une liste-type de toponymes (exonymes et endonymes) que l’on est en droit d’avoir par exemple sur une carte générale de Tunisie à moyenne échelle. -

Tunisia: Long-Term Solitary Confinement of Political Prisoners
TUNISIA: LONG-TERM SOLITARY CONFINEMENT OF POLITICAL PRISONERS Summary......................................................................................................................................... 1 Recommendations......................................................................................................................... 2 About this Report ......................................................................................................................... 4 Introduction................................................................................................................................... 6 Prison Conditions: Gradual Improvements............................................................................10 Pressures on Organizations and Journalists Reporting on Prison Conditions..................13 Prisoners in Isolation: Ten Cases..............................................................................................16 Solitary Confinement: International Norms and Health Consequences ............................24 Summary Tunisia’s policy of placing some of its more than 500 political prisoners in strict, long- term solitary confinement is one of the harshest holdovers from the prison regime of the 1990s, when conditions were worse overall. It threatens the mental health of the prisoners, denies them a means to challenge their being segregated, and violates international norms requiring that all persons in custody be treated with humanity and respect for their inherent dignity. Today between -

MPLS VPN Service
MPLS VPN Service PCCW Global’s MPLS VPN Service provides reliable and secure access to your network from anywhere in the world. This technology-independent solution enables you to handle a multitude of tasks ranging from mission-critical Enterprise Resource Planning (ERP), Customer Relationship Management (CRM), quality videoconferencing and Voice-over-IP (VoIP) to convenient email and web-based applications while addressing traditional network problems relating to speed, scalability, Quality of Service (QoS) management and traffic engineering. MPLS VPN enables routers to tag and forward incoming packets based on their class of service specification and allows you to run voice communications, video, and IT applications separately via a single connection and create faster and smoother pathways by simplifying traffic flow. Independent of other VPNs, your network enjoys a level of security equivalent to that provided by frame relay and ATM. Network diagram Database Customer Portal 24/7 online customer portal CE Router Voice Voice Regional LAN Headquarters Headquarters Data LAN Data LAN Country A LAN Country B PE CE Customer Router Service Portal PE Router Router • Router report IPSec • Traffic report Backup • QoS report PCCW Global • Application report MPLS Core Network Internet IPSec MPLS Gateway Partner Network PE Router CE Remote Router Site Access PE Router Voice CE Voice LAN Router Branch Office CE Data Branch Router Office LAN Country D Data LAN Country C Key benefits to your business n A fully-scalable solution requiring minimal investment -

En Outre, Le Laboratoire Central D'analyses Et D'essais Doit Détruire Les Vignettes Prévues Au Cours De L'année Écoulée Et
En outre, le laboratoire central d'analyses et Vu la loi n° 99-40 du 10 mai 1999, relative à la d'essais doit détruire les vignettes prévues au cours de métrologie légale, telle que modifiée et complétée par l'année écoulée et restantes en fin d'exercice et en la loi n° 2008-12 du 11 février 2008 et notamment ses informer par écrit l'agence nationale de métrologie articles 6,7 et 8, dans un délai ne dépassant pas la fin du mois de Vu le décret n° 2001-1036 du 8 mai 2001, fixant janvier de l’année qui suit. les modalités des contrôles métrologiques légaux, les Art. 8 - Le laboratoire central d'analyses et d'essais caractéristiques des marques de contrôle et les doit clairement mentionner sur la facture remise au conditions dans lesquelles elles sont apposées sur les demandeur de la vérification primitive ou de la instruments de mesure, notamment son article 42, vérification périodique des instruments de pesage à Vu le décret n° 2001-2965 du 20 décembre 2001, fonctionnement non automatique de portée maximale supérieure à 30 kilogrammes, le montant de la fixant les attributions du ministère du commerce, redevance à percevoir sur les opérations de contrôle Vu le décret n° 2008-2751 du 4 août 2008, fixant métrologique légal conformément aux dispositions du l’organisation administrative et financière de l’agence décret n° 2009-440 du 16 février 2009 susvisé. Le nationale de métrologie et les modalités de son montant de la redevance est assujetti à la taxe sur la fonctionnement, valeur ajoutée (TVA) de 18% conformément aux Vu le décret Présidentiel n° 2015-35 du 6 février règlements en vigueur. -

Section: ARIANA
Section: ARIANA Nom Prénom Adresse Code postal Tél ABDELMOULA AHMED 71,Avenue Habib Bourguiba 2080 ARIANA 71716297 ABDELMOUMEN EP, OUESLATI SOUMAYA Route Principale 7024 IMADA-ZOUAOUINE 72 403 525 ABDENNEBI EP, NAKOURI LILIA 14, Avenue de la Liberté C,C,Tej 1004 EL MENZAH 5 71 237 036 ALOULOU KHEDIJA Cité Commerciale Jamil 2080 ARIANA 71754731 AMARA EP, BEN RHOUMA ZOHRA 19, Rue Taieb M'Hiri 2041 CITE ETTADHAMEN 71 516 453 AMARA EP,MEDDEB CAMELIA Bezina 7012 BAZINA AMMAR EP,KRICHEN ZEINEB 44, Avenue Taieb M'Hiri 2080 ARIANA 71714659 AMRI MOHAMED NEJIB 11,Avenue Habib Bourguiba 1110 MORNAGUIA 71.540.255 ARBI ABDELAZIZ 19, Rue d'Algérie 7030 MATEUR 72485420 ARBI DALENDA 3, Rue d'Algérie 7050 MENZEL BOURGUIBA 72 460 219 AYADI MAHJOUB 15, Rue Musset-Ang rue Algérie 7050 MENZEL BOURGUIBA 72.463.768 AYADI EP, BEN HASSEN FADHILA 112, Avenue HabibBourguiba 2022 KALAAT EL ANDALOUS 71 558 423 AZAIEZ RIDHA Avenue Habib Bourguiba 1124 JEDEIDA 71539110 AZOUZ OLFA Résidence les Orangers- Av, des Orangers 2010 LA MANOUBA 71 603 755 AZOUZ EP, GHORBAL HAGER 1, Avenue de l'Environnement 2021 OUED ELLIL 71535301 AZOUZI EP, FERCHICHI RIM 57, Avenue Taieb M'Hiri 2041 CITE ETTADHAMEN 71 549 230 AZZOUZ ZOUHAIER 19, Avenue Emir Abdelkader- El Bhira 7000 BIZERTE 72 531 136 BACCOUCHE FERID 38, Avenue du 1er Mai 7000 BIZERTE 72 431 113 BAHRI RYM 61, Avenue Habib Bourguiba 7010 SEJNANE 7256114 BAKLOUTI EP, DJEMAL MERIAM Avenue 7 Novembre 7080 MENZEL JEMIL 72 490 600 BAKTACHE OTHMAN 19, Avenue Taieb M'Hiri 7000 BIZERTE 72 431 208 BANANI EP, M'ZAH AMENA 1, Rue de la -

Curriculum Vitae Mechanical Engineer
Curriculum Vitae Mechanical Engineer I. Public personal Information : Name: NAOUFEL YAHYAOUI. Date and place of birth: 03/02/1984 in TATAOUINE Nationality: Tunisian. Marital status: Married. Address: 3212 Bir lahmer West Tataouine, Tunisia. Mobile: (+216) 24 441 364 Email: [email protected] II. Academic curriculum: 2009: National Diploma in Mechanical Engineering. 2005-2009: Cycle Engineering at the National School of Engineers of Monastir: Mechanical Engineering. 2004-2005: diploma of University undergraduate Technologies. 2003-2005: Preparatory cycle, the Preparatory Institute for Engineering Studies of Monastir (ENIM), Technologies section. 2002-2003: Bachelor of Technology. III. Professional Experience: ❖ From September 2009 to June 2011: ▪ Employer : TUNICOM sa. ▪ Function : Responsible Production, then Responsible Management Quality. ▪ company’s activities : Metal construction( manufacturing bins,trays,equipment, Tanks) ❖ From August 2011 to April 2017: • Employer: MERI Engineering & Contruction. • Function: Mechanical Engineer [OIL AND GAS] • Company’s activities: Pipeline and Piping, pressure vessels and storage tanks, EPC Projects for Oil and Gas sector. • Mission: - DESIGN ENGINEER: ✓ Technical study to change coroner of Tank R1, R5, R13, R22 (TOTAL, TUNISIA). ✓ Study of manufacture of emulsifier tanks, tanks for JET A1 and vertical tanks for fuel (NAFTAL, ALGERIA). ✓ Study of the replacement of section of line N°03 DIESEL [Landing stage the Goulette OILLIBYA, Zone Oil Rades, TUNISIA). ✓ Design and installation of two fire water filters (Shell, TUNISIA). ✓ Study of Construction of two storage tanks of gasoline per unit of capacity 5000 m3 (CONGO-REFINERY, CORAF). ✓ Study of project: Loading /Off Loading stations & Metring Skids (THYNA PETROLEUM SERVICES –TPS, TUNISIA). ✓ Study of project: Acquisition and installation of an aviation fuel tank (AVGAS) of 50 m3 (School of Borj el Amri Aviation, Ministry of Army, Tunisia). -

L'averse Du 11 Avril 1989 Dans La Région De Tunis (Revue De La Presse Tunisienne De Langue Française)
L' A VER SE DU 1 1 AV R IL 1 9 a 9 D AN SLA R E G I 0 N DE T UN IS ( REVUI DI LA PRISSI 'fUIiSlllU DI LUGUI nUçAISI ) Avril 1989 1 1 1 1 AVANT-PROPOS 1 Une averse d'une grande intensité ,s'est abattue sur Tunis et sa banlieue dans 1 l'après-midi du mardi 11 avril 1989. L'épicentre de l'averse se trouvait quasiment à la verticale du quartier d'El Menzah 6 ,où nous avons 1 enregistré à notre pluviométre une hauteur de 87 mm entre 15h 10 t début de l'averse et 17h 15. A 19 heures la hauteur était de 104 mm et atteignait 122 mm. à 20h35 . Cette violente averse 1 orageuse , digne des plus belles tornades tropicales, accompagnée de vents violents a deversé sur les hauts quartiers d'El Menzah ,des 1 trombes d'eau et de grêle, qui ont très vite transformé rues et artères de ces quartiers en oueds impétueux , entrainant vers les zones basses des flots de boue et d'objets divers ! 1 Cette averse a occasionné des dégats importants , principalement dans le quartier de l'Ariana Nous avons rassemblé dans ce document l'ensemble 1 des articles relatant l'évènement dans les quotidiens de langue française . Nous lui avons joint une note élaborée par M. Ridha Kallel ,ainsi 1 que le bulletin pluviométrique quotidien du . 11 avril 1989,édité par le bureau d'annonce de crues 1 du B.I.R.H . 1 H.CAMUS 1 Directeur de Recherche ûRSTûM 1 1 1 1 1 1 1 METEO-------····-.--· 1 1 ·,·, -' ...... -

Gazoduc Borj El Amri Est De Mettre En Place L’Ensemble Des Mesures À Prendre En Urgence En Cas D'incident Lors De L'exploitation Du Gazoduc
+ Société Tunisienne d’Electricité et de Gaz Direction de la production et du transport du gaz Direction Equipement Gaz ************ ETUDE D’IMPACT SUR L’ENVIRONNEMENT ET ENQUETE PUBLIQUE POUR LE PROJET DE POSE DE CANALISATION DU GAZODUC D’ALIMENTATION EN GAZ NATUREL DE LA COMMUNE DE BORJ EL AMRI ETUDE D’IMPACT SUR L’ENVIRONNEMENT VERSION DEFINITIVE ROYAL INGENIEURIE "RIESG" -BP n° 69, Cité El Ghazela 2083 Ariana [email protected] EIE POUR LE PROJET DE POSE DU GAZODUC D’ALIMENTATION EN GAZ NATUREL DE LA COMMUNE DE BORJ EL AMRI TABLE DES MATIERES 1 Resume .............................................................................................................................. 5 2 Introduction ...................................................................................................................... 9 3 Cadre administratif, institutionnel et règlementaire .................................................. 10 3.1 Présentation de la société « STEG » ........................................................................ 10 3.2 Présentation du bureau d’études .............................................................................. 10 3.3 Cadre règlementaire ................................................................................................ 10 4 Présentation du projet de pose de gazoduc pour alimentation de la commune de Borj El Amri ........................................................................................................................... 12 4.1 Consistance du projet .............................................................................................. -
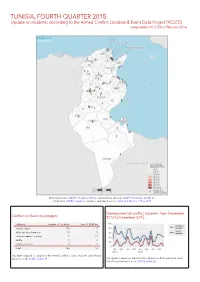
TUNISIA, FOURTH QUARTER 2015: Update on Incidents According to the Armed Conflict Location & Event Data Project (ACLED) Compiled by ACCORD, 4 February 2016
TUNISIA, FOURTH QUARTER 2015: Update on incidents according to the Armed Conflict Location & Event Data Project (ACLED) compiled by ACCORD, 4 February 2016 National borders: GADM, November 2015a; administrative divisions: GADM, November 2015b; in- cident data: ACLED, undated; coastlines and inland waters: Smith and Wessel, 1 May 2015 Development of conflict incidents from December Conflict incidents by category 2013 to December 2015 category number of incidents sum of fatalities riots/protests 118 3 strategic developments 10 0 violence against civilians 9 17 battle 4 4 remote violence 3 0 total 144 24 This table is based on data from the Armed Conflict Location & Event Data Project (datasets used: ACLED, undated). This graph is based on data from the Armed Conflict Location & Event Data Project (datasets used: ACLED, undated). TUNISIA, FOURTH QUARTER 2015: UPDATE ON INCIDENTS ACCORDING TO THE ARMED CONFLICT LOCATION & EVENT DATA PROJECT (ACLED) COMPILED BY ACCORD, 4 FEBRUARY 2016 LOCALIZATION OF CONFLICT INCIDENTS Note: The following list is an overview of the incident data included in the ACLED dataset. More details are available in the actual dataset (date, location data, event type, involved actors, information sources, etc.). In the following list, the names of event locations are taken from ACLED, while the administrative region names are taken from GADM data which serves as the basis for the map above. In Ben Arous (Tunis Sud), 1 incident killing 0 people was reported. The following location was affected: Ben Arous. In Bizerte, 2 incidents killing 0 people were reported. The following locations were affected: Bizerte, El Azib. In Béja, 1 incident killing 0 people was reported. -

„Um K WÒO U « WÒOMN*« WÒOFL'« WÒO U*« U
2 0 „uM�K� WO��u��« WOMN*« WOFL'« 0 Ò Ò Ò 8 WO�U*«Ò U��R*«ËÒ APTBEF TUNISIA’S PROFESSIONAL ASSOCIATION OF BANKS AND FINANCIAL INSTITUTIONS www.apbt.org.tnwww.apbt.org.tn Annual2008 report 2008 2009 E ّاجلمعية ّاملهنية ّالتونسية للبنوك ّواملؤسسات ّاملالية APTBEF TUNISIA’S PROFESSIONAL ASSOCIATION OF BANKS AND FINANCIAL INSTITUTIONS ANNUAL REPORT 2008 2009 ■ TUNISIA’S PROFESSIONAL ASSOCIATION OF BANKS AND FINANCIAL INSTITUTIONS www.apbt.org.tn PARTICIPANT MEMBERS LENDING INSTITUTIONS BANKS ■ AMEN BANK (AB) ■ ARAB BANKING CORPORATION (ABC) ■ ARAB TUNISIAN BANK (ATB) ■ ATTIJARI BANK OF TUNISIA (ATTIJARI BANK) ■ BANK FOR FINANCING SMALL/MEDIUM BUSINESSES (BFPME) ■ BANK OF HOUSING (BH) ■ BANK OF TUNISIA (BT) ■ TUNISIA AND EMIRATES BANK (BTE) ■ FRANCO-TUNISIAN BANK (BFT) ■ ARAB INTERNATIONAL BANK OF TUNISIA (BIAT) ■ NATIONAL AGRICULTURAL BANK (BNA) ■ TUNISIAN SOLIDARITY BANK (BTS) ■ TUNISO-KUWAITI BANK (BTK) ■ TUNISO-LIBYAN BANK (BTL) ■ CITIBANK ■ TUNISIAN BANKING COMPANY (STB) ■ STUSID BANK ■ TUNISIAN QATARI BANK (TQB) ■ BANKING UNION FOR TRADE AND INDUSTRY (UBCI) ■ INTERNATIONAL BANKING UNION (UIB). 2 TUNISIA’S PROFESSIONAL ASSOCIATION OF BANKS AND FINANCIAL INSTITUTIONS ■ FINANCIAL INSTITUTIONS www.apbt.org.tn LEASING COMPANIES ■ ARAB INTERNATIONAL LEASE ■ ARAB TUNISIAN LEASE ■ ATTIJARI LEASING ■ LEASING INTERNATIONAL COMPANY ■ EL WIFACK LEASING ■ HANNIBAL LEASE ■ MODERN LEASING ■ TUNISIA LEASING ■ UBCI LEASING. FACTORING COMPANIES ■ TUNISIA FACTORING ■ UNIFACTOR. OTHER MEMBERS ■ BANK ETTAMOUIL TOUNSI SAOUDI (BEST BANK) ■ TUNISIA MERCHANT BANK (BAT) ■ NORTH AFRICA INTERNATIONAL BANK (NAIB) ■ TUNISIAN UNION OF BANKS (UTB). ASSOCIATE MEMBERS ■ ARAB INTERNATIONAL COLLECTION COMPANY ■ INTERNATIONAL CLAIM COLLECTION ■ EL ISTIFA COMPANY ■ FINANCIAL CLAIM COLLECTION COMPANY ■ GENERAL CLAIM COLLECTION COMPANY ■ RAPID COLLECTION COMPANY ■ TUNISIAN CLAIM COLLECTION COMPANY ■ SOUTHERN COLLECTION.