The Molecular and Functional Analyses of Neurochondrin Mouse Mutant
Total Page:16
File Type:pdf, Size:1020Kb
Load more
Recommended publications
-

A Comparative Analysis of Transcribed Genes in the Mouse Hypothalamus and Neocortex Reveals Chromosomal Clustering
A comparative analysis of transcribed genes in the mouse hypothalamus and neocortex reveals chromosomal clustering Wee-Ming Boon*, Tim Beissbarth†, Lavinia Hyde†, Gordon Smyth†, Jenny Gunnersen*, Derek A. Denton*‡, Hamish Scott†, and Seong-Seng Tan* *Howard Florey Institute, University of Melbourne, Parkville 3052, Australia; and †Genetics and Bioinfomatics Division, Walter and Eliza Hall Institute of Medical Research, Royal Parade, Parkville 3050, Australia Contributed by Derek A. Denton, August 26, 2004 The hypothalamus and neocortex are subdivisions of the mamma- representing all of the genes that are expressed (qualitative and lian forebrain, and yet, they have vastly different evolutionary quantitative) in the hypothalamus and neocortex under standard histories, cytoarchitecture, and biological functions. In an attempt conditions. to define these attributes in terms of their genetic activity, we have In the current study, we describe the use of the Serial Analysis compared their genetic repertoires by using the Serial Analysis of of Gene Expression (SAGE) database, which allows simulta- Gene Expression database. From a comparison of 78,784 hypothal- neous detection of the expression levels of the entire genome amus tags with 125,296 neocortical tags, we demonstrate that each without a priori knowledge of gene sequences (13). SAGE takes structure possesses a different transcriptional profile in terms of advantage of the fact that a small sequence tag taken from a gene ontological characteristics and expression levels. Despite its defined position within the transcript is sufficient to identify the more recent evolutionary history, the neocortex has a more com- gene (from known cDNA or EST sequences), and up to 40 tags plex pattern of gene activity. -

Supplementary Table 1: Adhesion Genes Data Set
Supplementary Table 1: Adhesion genes data set PROBE Entrez Gene ID Celera Gene ID Gene_Symbol Gene_Name 160832 1 hCG201364.3 A1BG alpha-1-B glycoprotein 223658 1 hCG201364.3 A1BG alpha-1-B glycoprotein 212988 102 hCG40040.3 ADAM10 ADAM metallopeptidase domain 10 133411 4185 hCG28232.2 ADAM11 ADAM metallopeptidase domain 11 110695 8038 hCG40937.4 ADAM12 ADAM metallopeptidase domain 12 (meltrin alpha) 195222 8038 hCG40937.4 ADAM12 ADAM metallopeptidase domain 12 (meltrin alpha) 165344 8751 hCG20021.3 ADAM15 ADAM metallopeptidase domain 15 (metargidin) 189065 6868 null ADAM17 ADAM metallopeptidase domain 17 (tumor necrosis factor, alpha, converting enzyme) 108119 8728 hCG15398.4 ADAM19 ADAM metallopeptidase domain 19 (meltrin beta) 117763 8748 hCG20675.3 ADAM20 ADAM metallopeptidase domain 20 126448 8747 hCG1785634.2 ADAM21 ADAM metallopeptidase domain 21 208981 8747 hCG1785634.2|hCG2042897 ADAM21 ADAM metallopeptidase domain 21 180903 53616 hCG17212.4 ADAM22 ADAM metallopeptidase domain 22 177272 8745 hCG1811623.1 ADAM23 ADAM metallopeptidase domain 23 102384 10863 hCG1818505.1 ADAM28 ADAM metallopeptidase domain 28 119968 11086 hCG1786734.2 ADAM29 ADAM metallopeptidase domain 29 205542 11085 hCG1997196.1 ADAM30 ADAM metallopeptidase domain 30 148417 80332 hCG39255.4 ADAM33 ADAM metallopeptidase domain 33 140492 8756 hCG1789002.2 ADAM7 ADAM metallopeptidase domain 7 122603 101 hCG1816947.1 ADAM8 ADAM metallopeptidase domain 8 183965 8754 hCG1996391 ADAM9 ADAM metallopeptidase domain 9 (meltrin gamma) 129974 27299 hCG15447.3 ADAMDEC1 ADAM-like, -

Open Data for Differential Network Analysis in Glioma
International Journal of Molecular Sciences Article Open Data for Differential Network Analysis in Glioma , Claire Jean-Quartier * y , Fleur Jeanquartier y and Andreas Holzinger Holzinger Group HCI-KDD, Institute for Medical Informatics, Statistics and Documentation, Medical University Graz, Auenbruggerplatz 2/V, 8036 Graz, Austria; [email protected] (F.J.); [email protected] (A.H.) * Correspondence: [email protected] These authors contributed equally to this work. y Received: 27 October 2019; Accepted: 3 January 2020; Published: 15 January 2020 Abstract: The complexity of cancer diseases demands bioinformatic techniques and translational research based on big data and personalized medicine. Open data enables researchers to accelerate cancer studies, save resources and foster collaboration. Several tools and programming approaches are available for analyzing data, including annotation, clustering, comparison and extrapolation, merging, enrichment, functional association and statistics. We exploit openly available data via cancer gene expression analysis, we apply refinement as well as enrichment analysis via gene ontology and conclude with graph-based visualization of involved protein interaction networks as a basis for signaling. The different databases allowed for the construction of huge networks or specified ones consisting of high-confidence interactions only. Several genes associated to glioma were isolated via a network analysis from top hub nodes as well as from an outlier analysis. The latter approach highlights a mitogen-activated protein kinase next to a member of histondeacetylases and a protein phosphatase as genes uncommonly associated with glioma. Cluster analysis from top hub nodes lists several identified glioma-associated gene products to function within protein complexes, including epidermal growth factors as well as cell cycle proteins or RAS proto-oncogenes. -
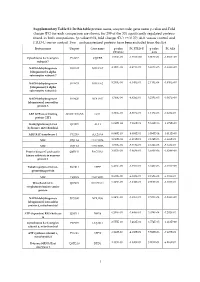
In This Table Protein Name, Uniprot Code, Gene Name P-Value
Supplementary Table S1: In this table protein name, uniprot code, gene name p-value and Fold change (FC) for each comparison are shown, for 299 of the 301 significantly regulated proteins found in both comparisons (p-value<0.01, fold change (FC) >+/-0.37) ALS versus control and FTLD-U versus control. Two uncharacterized proteins have been excluded from this list Protein name Uniprot Gene name p value FC FTLD-U p value FC ALS FTLD-U ALS Cytochrome b-c1 complex P14927 UQCRB 1.534E-03 -1.591E+00 6.005E-04 -1.639E+00 subunit 7 NADH dehydrogenase O95182 NDUFA7 4.127E-04 -9.471E-01 3.467E-05 -1.643E+00 [ubiquinone] 1 alpha subcomplex subunit 7 NADH dehydrogenase O43678 NDUFA2 3.230E-04 -9.145E-01 2.113E-04 -1.450E+00 [ubiquinone] 1 alpha subcomplex subunit 2 NADH dehydrogenase O43920 NDUFS5 1.769E-04 -8.829E-01 3.235E-05 -1.007E+00 [ubiquinone] iron-sulfur protein 5 ARF GTPase-activating A0A0C4DGN6 GIT1 1.306E-03 -8.810E-01 1.115E-03 -7.228E-01 protein GIT1 Methylglutaconyl-CoA Q13825 AUH 6.097E-04 -7.666E-01 5.619E-06 -1.178E+00 hydratase, mitochondrial ADP/ATP translocase 1 P12235 SLC25A4 6.068E-03 -6.095E-01 3.595E-04 -1.011E+00 MIC J3QTA6 CHCHD6 1.090E-04 -5.913E-01 2.124E-03 -5.948E-01 MIC J3QTA6 CHCHD6 1.090E-04 -5.913E-01 2.124E-03 -5.948E-01 Protein kinase C and casein Q9BY11 PACSIN1 3.837E-03 -5.863E-01 3.680E-06 -1.824E+00 kinase substrate in neurons protein 1 Tubulin polymerization- O94811 TPPP 6.466E-03 -5.755E-01 6.943E-06 -1.169E+00 promoting protein MIC C9JRZ6 CHCHD3 2.912E-02 -6.187E-01 2.195E-03 -9.781E-01 Mitochondrial 2- -

SZDB: a Database for Schizophrenia Genetic Research
Schizophrenia Bulletin vol. 43 no. 2 pp. 459–471, 2017 doi:10.1093/schbul/sbw102 Advance Access publication July 22, 2016 SZDB: A Database for Schizophrenia Genetic Research Yong Wu1,2, Yong-Gang Yao1–4, and Xiong-Jian Luo*,1,2,4 1Key Laboratory of Animal Models and Human Disease Mechanisms of the Chinese Academy of Sciences and Yunnan Province, Kunming Institute of Zoology, Kunming, China; 2Kunming College of Life Science, University of Chinese Academy of Sciences, Kunming, China; 3CAS Center for Excellence in Brain Science and Intelligence Technology, Chinese Academy of Sciences, Shanghai, China 4YGY and XJL are co-corresponding authors who jointly directed this work. *To whom correspondence should be addressed; Kunming Institute of Zoology, Chinese Academy of Sciences, Kunming, Yunnan 650223, China; tel: +86-871-68125413, fax: +86-871-68125413, e-mail: [email protected] Schizophrenia (SZ) is a debilitating brain disorder with a Introduction complex genetic architecture. Genetic studies, especially Schizophrenia (SZ) is a severe mental disorder charac- recent genome-wide association studies (GWAS), have terized by abnormal perceptions, incoherent or illogi- identified multiple variants (loci) conferring risk to SZ. cal thoughts, and disorganized speech and behavior. It However, how to efficiently extract meaningful biological affects approximately 0.5%–1% of the world populations1 information from bulk genetic findings of SZ remains a and is one of the leading causes of disability worldwide.2–4 major challenge. There is a pressing -

Generation of Induced Pluripotent Stem Cells (Ipscs) Lines Deficient for Genes Associated with Neurodevelopmental Diseases Using CRISPR/Cas9 Technology
Generation of induced pluripotent stem cells (iPSCs) lines deficient for genes associated with neurodevelopmental diseases using CRISPR/Cas9 technology Claudia De Guidi Degree project in biology, Master of science (2 years), 2021 Examensarbete i biologi 45 hp till masterexamen, 2021 Biology Education Centre and Department of Immunology, Genetics and Pathology, Science for Life Laboratory, Uppsala University Supervisor: Jens Schuster External opponent: Josefin Johansson Table of Contents Abstract ............................................................................................................................................ 3 List of abbreviations ..................................................................................................................... 4 1 Introduction ........................................................................................................................ 5 1.1 Characteristics and applications of Induced pluripotent stem cells (iPSCs). ........... 5 1.2 Neurodevelopmental disorders ............................................................................................ 6 1.3 Aim of the study ....................................................................................................................... 7 2 Materials and methods ..................................................................................................... 7 2.1 Culture of iPSC lines .............................................................................................................. 7 2.2 -

Supplemental Figure 1. Protein-Protein Interaction Network with Increased Expression in Fteb During the Luteal Phase
Supplemental Figure 1. Protein-protein interaction network with increased expression in FTEb during the luteal phase. Supplemental Figure 2. Protein-protein interaction network with decreased expression in FTEb during luteal phase. LEGENDS TO SUPPLEMENTAL FIGURES Supplemental Figure 1. Protein-protein interaction network with increased expression in FTEb during the luteal phase. Submission of probe sets differentially expressed in the FTEb specimens that clustered with SerCa as well as those specifically altered in FTEb luteal samples to the online I2D database revealed overlapping networks of proteins with increased expression in the four FTEb samples and/or FTEb luteal samples overall. Proteins are represented by nodes, and known and predicted first-degree interactions are represented by solid lines. Genes encoding proteins shown as large ovals highlighted in blue were exclusively found in the first comparison (Manuscript Figure 2), whereas those highlighted in red were only found in the second comparison (Manuscript Figure 3). Genes encoding proteins shown as large ovals highlighted in black were found in both comparisons. The color of each node indicates the ontology of the corresponding protein as determined by the Online Predicted Human Interaction Database (OPHID) link with the NAViGaTOR software. Supplemental Figure 2. Protein-protein interaction network with decreased expression in FTEb during the luteal phase. Submission of probe sets differentially expressed in the FTEb specimens that clustered with SerCa as well as those specifically altered in FTEb luteal samples to the online I2D database revealed overlapping networks of proteins with decreased expression in the four FTEb samples and/or FTEb luteal samples overall. Proteins are represented by nodes, and known and predicted first-degree interactions are represented by solid lines. -

(12) Patent Application Publication (10) Pub. No.: US 2016/0264934 A1 GALLOURAKIS Et Al
US 20160264934A1 (19) United States (12) Patent Application Publication (10) Pub. No.: US 2016/0264934 A1 GALLOURAKIS et al. (43) Pub. Date: Sep. 15, 2016 (54) METHODS FOR MODULATING AND Publication Classification ASSAYING MI6AIN STEM CELL POPULATIONS (51) Int. Cl. CI2N5/0735 (2006.01) (71) Applicants: THE GENERAL, HOSPITAL AOIN I/02 (2006.01) CORPORATION, Boston, MA (US); CI2O I/68 (2006.01) The Regents of the University of GOIN 33/573 (2006.01) California, Oakland, CA (US) CI2N 5/077 (2006.01) CI2N5/0793 (2006.01) (72) Inventors: Cosmas GIALLOURAKIS, Boston, (52) U.S. Cl. MA (US); Alan C. MULLEN, CPC ............ CI2N5/0606 (2013.01); CI2N5/0657 Brookline, MA (US); Yi XING, (2013.01); C12N5/0619 (2013.01); C12O Torrance, CA (US) I/6888 (2013.01); G0IN33/573 (2013.01); A0IN I/0226 (2013.01); C12N 2501/72 (73) Assignees: THE GENERAL, HOSPITAL (2013.01); C12N 2506/02 (2013.01); C12O CORPORATION, Boston, MA (US); 2600/158 (2013.01); C12Y 201/01062 The Regents of the University of (2013.01); C12Y 201/01 (2013.01) California, Oakland, CA (US) (57) ABSTRACT (21) Appl. No.: 15/067,780 The present invention generally relates to methods, assays and kits to maintain a human stem cell population in an (22) Filed: Mar 11, 2016 undifferentiated state by inhibiting the expression or function of METTL3 and/or METTL4, and mA fingerprint methods, assays, arrays and kits to assess the cell state of a human stem Related U.S. Application Data cell population by assessing mA levels (e.g. mA peak inten (60) Provisional application No. -

The Changing Chromatome As a Driver of Disease: a Panoramic View from Different Methodologies
The changing chromatome as a driver of disease: A panoramic view from different methodologies Isabel Espejo1, Luciano Di Croce,1,2,3 and Sergi Aranda1 1. Centre for Genomic Regulation (CRG), Barcelona Institute of Science and Technology, Dr. Aiguader 88, Barcelona 08003, Spain 2. Universitat Pompeu Fabra (UPF), Barcelona, Spain 3. ICREA, Pg. Lluis Companys 23, Barcelona 08010, Spain *Corresponding authors: Luciano Di Croce ([email protected]) Sergi Aranda ([email protected]) 1 GRAPHICAL ABSTRACT Chromatin-bound proteins regulate gene expression, replicate and repair DNA, and transmit epigenetic information. Several human diseases are highly influenced by alterations in the chromatin- bound proteome. Thus, biochemical approaches for the systematic characterization of the chromatome could contribute to identifying new regulators of cellular functionality, including those that are relevant to human disorders. 2 SUMMARY Chromatin-bound proteins underlie several fundamental cellular functions, such as control of gene expression and the faithful transmission of genetic and epigenetic information. Components of the chromatin proteome (the “chromatome”) are essential in human life, and mutations in chromatin-bound proteins are frequently drivers of human diseases, such as cancer. Proteomic characterization of chromatin and de novo identification of chromatin interactors could thus reveal important and perhaps unexpected players implicated in human physiology and disease. Recently, intensive research efforts have focused on developing strategies to characterize the chromatome composition. In this review, we provide an overview of the dynamic composition of the chromatome, highlight the importance of its alterations as a driving force in human disease (and particularly in cancer), and discuss the different approaches to systematically characterize the chromatin-bound proteome in a global manner. -

Systems Genetics in Diversity Outbred Mice Inform BMD GWAS and Identify Determinants of Bone Strength
ARTICLE https://doi.org/10.1038/s41467-021-23649-0 OPEN Systems genetics in diversity outbred mice inform BMD GWAS and identify determinants of bone strength Basel M. Al-Barghouthi 1,2,8, Larry D. Mesner1,3,8, Gina M. Calabrese1,8, Daniel Brooks4, Steven M. Tommasini 5, Mary L. Bouxsein 4, Mark C. Horowitz5, Clifford J. Rosen 6, Kevin Nguyen1, ✉ Samuel Haddox2, Emily A. Farber1, Suna Onengut-Gumuscu 1,3, Daniel Pomp7 & Charles R. Farber 1,2,3 1234567890():,; Genome-wide association studies (GWASs) for osteoporotic traits have identified over 1000 associations; however, their impact has been limited by the difficulties of causal gene iden- tification and a strict focus on bone mineral density (BMD). Here, we use Diversity Outbred (DO) mice to directly address these limitations by performing a systems genetics analysis of 55 complex skeletal phenotypes. We apply a network approach to cortical bone RNA-seq data to discover 66 genes likely to be causal for human BMD GWAS associations, including the genes SERTAD4 and GLT8D2. We also perform GWAS in the DO for a wide-range of bone traits and identify Qsox1 as a gene influencing cortical bone accrual and bone strength. In this work, we advance our understanding of the genetics of osteoporosis and highlight the ability of the mouse to inform human genetics. 1 Center for Public Health Genomics, School of Medicine, University of Virginia, Charlottesville, VA, USA. 2 Department of Biochemistry and Molecular Genetics, School of Medicine, University of Virginia, Charlottesville, VA, USA. 3 Department of Public Health Sciences, School of Medicine, University of Virginia, Charlottesville, VA, USA. -

Identification of Acquired Copy Number Alterations and Uniparental
Leukemia (2010) 24, 438–449 & 2010 Macmillan Publishers Limited All rights reserved 0887-6924/10 $32.00 www.nature.com/leu ORIGINAL ARTICLE Identification of acquired copy number alterations and uniparental disomies in cytogenetically normal acute myeloid leukemia using high-resolution single-nucleotide polymorphism analysis L Bullinger1,4, J Kro¨nke1,4, C Scho¨n1,4, I Radtke2, K Urlbauer1, U Botzenhardt1, V Gaidzik1, A Cario´ 1, C Senger1, RF Schlenk1, JR Downing2, K Holzmann3,KDo¨hner1 and H Do¨hner1 1Department of Internal Medicine III, University Hospital of Ulm, Ulm, Germany; 2Department of Pathology, St Jude Children’s Research Hospital, Memphis, TN, USA and 3Microarray Core Facility, University of Ulm, Ulm, Germany Recent advances in genome-wide single-nucleotide polymorph- tyrosine kinase 3 (FLT3) gene the CCAAT/enhancer binding ism (SNP) analyses have revealed previously unrecognized protein-a (CEBPA) gene, the myeloid-lymphoid or mixed-line- microdeletions and uniparental disomy (UPD) in a broad age leukemia (MLL) gene, the neuroblastoma RAS viral spectrum of human cancers. As acute myeloid leukemia (AML) represents a genetically heterogeneous disease, this oncogene homolog (NRAS) gene, the Wilms’ tumor 1 (WT1) technology might prove helpful, especially for cytogenetically gene, and the runt-related transcription factor 1 (RUNX1) 4,5 normal AML (CN-AML) cases. Thus, we performed high- gene. These aberrations underscore the genetic complexity resolution SNP analyses in 157 adult cases of CN-AML. Regions of CN-AML and many additional genetic lesions are expected to of acquired UPDs were identified in 12% of cases and in the be present in this subset of AML. -

Neurochondrin (NCDN) Rabbit Polyclonal Antibody Product Data
OriGene Technologies, Inc. 9620 Medical Center Drive, Ste 200 Rockville, MD 20850, US Phone: +1-888-267-4436 [email protected] EU: [email protected] CN: [email protected] Product datasheet for AP55103SU-N Neurochondrin (NCDN) Rabbit Polyclonal Antibody Product data: Product Type: Primary Antibodies Applications: ELISA, IHC, WB Recommended Dilution: ELISA. Western Blot. Immunohistochemistry. Reactivity: Human Host: Rabbit Clonality: Polyclonal Immunogen: Synthetic peptides derived from N-terminal part of the Human Norbin protein. Specificity: This antibody reacts with Human 79 kDa protein. Formulation: State: Serum State: Lyophilized serum Preservative: None Reconstitution Method: Restore in distilled water. Conjugation: Unconjugated Storage: Prior to reconstitution store the antibody at -20°C. Store the reconstituted antibody at 2-8°C for one month or (in aliquots) at -20°C for longer. Avoid repeated freezing and thawing. Stability: Shelf life: one year from despatch. Database Link: Entrez Gene 23154 Human Q9UBB6 This product is to be used for laboratory only. Not for diagnostic or therapeutic use. View online » ©2021 OriGene Technologies, Inc., 9620 Medical Center Drive, Ste 200, Rockville, MD 20850, US 1 / 2 Neurochondrin (NCDN) Rabbit Polyclonal Antibody – AP55103SU-N Background: Norbin, also known as Neurochondrin, is a neuron-specific cytoplasmic protein involved in dendrite outgrowth. Overexpression of norbin in cultured Neuro 2a cells induced neurite- outgrowth. Norbin is located at rat chromosome 5q36. In addition to its involvement in dendrite outgrowth, Norbin is implicated in neural plasticity, chondrocyte differentiation, and early embryogenesis and in bone metabolism by inducing bone marrow cells to absorb bone matrix. Norbin is also an important endogenous modulator of metabotropic glutamate receptor 5 (mGluR5).