Is ARPC5 Required for Maintaining the Equilibrium Between Cancer Stem Cells and Non-Stem Cancer Cells?
Total Page:16
File Type:pdf, Size:1020Kb
Load more
Recommended publications
-

Biomarker Discovery for Chronic Liver Diseases by Multi-Omics
www.nature.com/scientificreports OPEN Biomarker discovery for chronic liver diseases by multi-omics – a preclinical case study Daniel Veyel1, Kathrin Wenger1, Andre Broermann2, Tom Bretschneider1, Andreas H. Luippold1, Bartlomiej Krawczyk1, Wolfgang Rist 1* & Eric Simon3* Nonalcoholic steatohepatitis (NASH) is a major cause of liver fbrosis with increasing prevalence worldwide. Currently there are no approved drugs available. The development of new therapies is difcult as diagnosis and staging requires biopsies. Consequently, predictive plasma biomarkers would be useful for drug development. Here we present a multi-omics approach to characterize the molecular pathophysiology and to identify new plasma biomarkers in a choline-defcient L-amino acid-defned diet rat NASH model. We analyzed liver samples by RNA-Seq and proteomics, revealing disease relevant signatures and a high correlation between mRNA and protein changes. Comparison to human data showed an overlap of infammatory, metabolic, and developmental pathways. Using proteomics analysis of plasma we identifed mainly secreted proteins that correlate with liver RNA and protein levels. We developed a multi-dimensional attribute ranking approach integrating multi-omics data with liver histology and prior knowledge uncovering known human markers, but also novel candidates. Using regression analysis, we show that the top-ranked markers were highly predictive for fbrosis in our model and hence can serve as preclinical plasma biomarkers. Our approach presented here illustrates the power of multi-omics analyses combined with plasma proteomics and is readily applicable to human biomarker discovery. Nonalcoholic fatty liver disease (NAFLD) is the major liver disease in western countries and is ofen associated with obesity, metabolic syndrome, or type 2 diabetes. -

Mitoxplorer, a Visual Data Mining Platform To
mitoXplorer, a visual data mining platform to systematically analyze and visualize mitochondrial expression dynamics and mutations Annie Yim, Prasanna Koti, Adrien Bonnard, Fabio Marchiano, Milena Dürrbaum, Cecilia Garcia-Perez, José Villaveces, Salma Gamal, Giovanni Cardone, Fabiana Perocchi, et al. To cite this version: Annie Yim, Prasanna Koti, Adrien Bonnard, Fabio Marchiano, Milena Dürrbaum, et al.. mitoXplorer, a visual data mining platform to systematically analyze and visualize mitochondrial expression dy- namics and mutations. Nucleic Acids Research, Oxford University Press, 2020, 10.1093/nar/gkz1128. hal-02394433 HAL Id: hal-02394433 https://hal-amu.archives-ouvertes.fr/hal-02394433 Submitted on 4 Dec 2019 HAL is a multi-disciplinary open access L’archive ouverte pluridisciplinaire HAL, est archive for the deposit and dissemination of sci- destinée au dépôt et à la diffusion de documents entific research documents, whether they are pub- scientifiques de niveau recherche, publiés ou non, lished or not. The documents may come from émanant des établissements d’enseignement et de teaching and research institutions in France or recherche français ou étrangers, des laboratoires abroad, or from public or private research centers. publics ou privés. Distributed under a Creative Commons Attribution| 4.0 International License Nucleic Acids Research, 2019 1 doi: 10.1093/nar/gkz1128 Downloaded from https://academic.oup.com/nar/advance-article-abstract/doi/10.1093/nar/gkz1128/5651332 by Bibliothèque de l'université la Méditerranée user on 04 December 2019 mitoXplorer, a visual data mining platform to systematically analyze and visualize mitochondrial expression dynamics and mutations Annie Yim1,†, Prasanna Koti1,†, Adrien Bonnard2, Fabio Marchiano3, Milena Durrbaum¨ 1, Cecilia Garcia-Perez4, Jose Villaveces1, Salma Gamal1, Giovanni Cardone1, Fabiana Perocchi4, Zuzana Storchova1,5 and Bianca H. -

A Bioinformatics Tool for Prioritizing Biological Leads from ‘Omics Data Using Literature Retrieval and Data Mining
International Journal of Molecular Sciences Article OmixLitMiner: A Bioinformatics Tool for Prioritizing Biological Leads from ‘Omics Data Using Literature Retrieval and Data Mining Pascal Steffen 1,2,3 , Jemma Wu 2, Shubhang Hariharan 1, Hannah Voss 3, Vijay Raghunath 4, Mark P. Molloy 1,2,* and Hartmut Schlüter 3,* 1 Bowel Cancer and Biomarker Research, Kolling Institute, The University of Sydney, Sydney 2065, Australia; pascal.steff[email protected] (P.S.); [email protected] (S.H.) 2 Department of Molecular Sciences, Macquarie University, Sydney 2109, Australia; [email protected] 3 Mass Spectrometric Proteomics Group, Department of Clinical Chemistry and Laboratory Medicine, University Medical Center Hamburg-Eppendorf (UKE), Hamburg 20246, Germany; [email protected] 4 Sydney Informatics Hub, The University of Sydney, Sydney 2008, Australia; [email protected] * Correspondence: [email protected] (M.P.M.); [email protected] (H.S.) Received: 7 November 2019; Accepted: 13 February 2020; Published: 19 February 2020 Abstract: Proteomics and genomics discovery experiments generate increasingly large result tables, necessitating more researcher time to convert the biological data into new knowledge. Literature review is an important step in this process and can be tedious for large scale experiments. An informed and strategic decision about which biomolecule targets should be pursued for follow-up experiments thus remains a considerable challenge. To streamline and formalise this process of literature retrieval and analysis of discovery based ‘omics data and as a decision-facilitating support tool for follow-up experiments we present OmixLitMiner, a package written in the computational language R. The tool automates the retrieval of literature from PubMed based on UniProt protein identifiers, gene names and their synonyms, combined with user defined contextual keyword search (i.e., gene ontology based). -

Supplementary Table 3: Genes Only Influenced By
Supplementary Table 3: Genes only influenced by X10 Illumina ID Gene ID Entrez Gene Name Fold change compared to vehicle 1810058M03RIK -1.104 2210008F06RIK 1.090 2310005E10RIK -1.175 2610016F04RIK 1.081 2610029K11RIK 1.130 381484 Gm5150 predicted gene 5150 -1.230 4833425P12RIK -1.127 4933412E12RIK -1.333 6030458P06RIK -1.131 6430550H21RIK 1.073 6530401D06RIK 1.229 9030607L17RIK -1.122 A330043C08RIK 1.113 A330043L12 1.054 A530092L01RIK -1.069 A630054D14 1.072 A630097D09RIK -1.102 AA409316 FAM83H family with sequence similarity 83, member H 1.142 AAAS AAAS achalasia, adrenocortical insufficiency, alacrimia 1.144 ACADL ACADL acyl-CoA dehydrogenase, long chain -1.135 ACOT1 ACOT1 acyl-CoA thioesterase 1 -1.191 ADAMTSL5 ADAMTSL5 ADAMTS-like 5 1.210 AFG3L2 AFG3L2 AFG3 ATPase family gene 3-like 2 (S. cerevisiae) 1.212 AI256775 RFESD Rieske (Fe-S) domain containing 1.134 Lipo1 (includes AI747699 others) lipase, member O2 -1.083 AKAP8L AKAP8L A kinase (PRKA) anchor protein 8-like -1.263 AKR7A5 -1.225 AMBP AMBP alpha-1-microglobulin/bikunin precursor 1.074 ANAPC2 ANAPC2 anaphase promoting complex subunit 2 -1.134 ANKRD1 ANKRD1 ankyrin repeat domain 1 (cardiac muscle) 1.314 APOA1 APOA1 apolipoprotein A-I -1.086 ARHGAP26 ARHGAP26 Rho GTPase activating protein 26 -1.083 ARL5A ARL5A ADP-ribosylation factor-like 5A -1.212 ARMC3 ARMC3 armadillo repeat containing 3 -1.077 ARPC5 ARPC5 actin related protein 2/3 complex, subunit 5, 16kDa -1.190 activating transcription factor 4 (tax-responsive enhancer element ATF4 ATF4 B67) 1.481 AU014645 NCBP1 nuclear cap -

Role and Regulation of the P53-Homolog P73 in the Transformation of Normal Human Fibroblasts
Role and regulation of the p53-homolog p73 in the transformation of normal human fibroblasts Dissertation zur Erlangung des naturwissenschaftlichen Doktorgrades der Bayerischen Julius-Maximilians-Universität Würzburg vorgelegt von Lars Hofmann aus Aschaffenburg Würzburg 2007 Eingereicht am Mitglieder der Promotionskommission: Vorsitzender: Prof. Dr. Dr. Martin J. Müller Gutachter: Prof. Dr. Michael P. Schön Gutachter : Prof. Dr. Georg Krohne Tag des Promotionskolloquiums: Doktorurkunde ausgehändigt am Erklärung Hiermit erkläre ich, dass ich die vorliegende Arbeit selbständig angefertigt und keine anderen als die angegebenen Hilfsmittel und Quellen verwendet habe. Diese Arbeit wurde weder in gleicher noch in ähnlicher Form in einem anderen Prüfungsverfahren vorgelegt. Ich habe früher, außer den mit dem Zulassungsgesuch urkundlichen Graden, keine weiteren akademischen Grade erworben und zu erwerben gesucht. Würzburg, Lars Hofmann Content SUMMARY ................................................................................................................ IV ZUSAMMENFASSUNG ............................................................................................. V 1. INTRODUCTION ................................................................................................. 1 1.1. Molecular basics of cancer .......................................................................................... 1 1.2. Early research on tumorigenesis ................................................................................. 3 1.3. Developing -
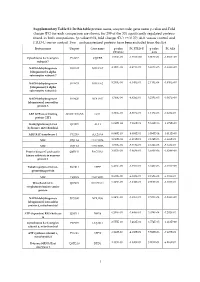
In This Table Protein Name, Uniprot Code, Gene Name P-Value
Supplementary Table S1: In this table protein name, uniprot code, gene name p-value and Fold change (FC) for each comparison are shown, for 299 of the 301 significantly regulated proteins found in both comparisons (p-value<0.01, fold change (FC) >+/-0.37) ALS versus control and FTLD-U versus control. Two uncharacterized proteins have been excluded from this list Protein name Uniprot Gene name p value FC FTLD-U p value FC ALS FTLD-U ALS Cytochrome b-c1 complex P14927 UQCRB 1.534E-03 -1.591E+00 6.005E-04 -1.639E+00 subunit 7 NADH dehydrogenase O95182 NDUFA7 4.127E-04 -9.471E-01 3.467E-05 -1.643E+00 [ubiquinone] 1 alpha subcomplex subunit 7 NADH dehydrogenase O43678 NDUFA2 3.230E-04 -9.145E-01 2.113E-04 -1.450E+00 [ubiquinone] 1 alpha subcomplex subunit 2 NADH dehydrogenase O43920 NDUFS5 1.769E-04 -8.829E-01 3.235E-05 -1.007E+00 [ubiquinone] iron-sulfur protein 5 ARF GTPase-activating A0A0C4DGN6 GIT1 1.306E-03 -8.810E-01 1.115E-03 -7.228E-01 protein GIT1 Methylglutaconyl-CoA Q13825 AUH 6.097E-04 -7.666E-01 5.619E-06 -1.178E+00 hydratase, mitochondrial ADP/ATP translocase 1 P12235 SLC25A4 6.068E-03 -6.095E-01 3.595E-04 -1.011E+00 MIC J3QTA6 CHCHD6 1.090E-04 -5.913E-01 2.124E-03 -5.948E-01 MIC J3QTA6 CHCHD6 1.090E-04 -5.913E-01 2.124E-03 -5.948E-01 Protein kinase C and casein Q9BY11 PACSIN1 3.837E-03 -5.863E-01 3.680E-06 -1.824E+00 kinase substrate in neurons protein 1 Tubulin polymerization- O94811 TPPP 6.466E-03 -5.755E-01 6.943E-06 -1.169E+00 promoting protein MIC C9JRZ6 CHCHD3 2.912E-02 -6.187E-01 2.195E-03 -9.781E-01 Mitochondrial 2- -

HMMR Acts in the PLK1-Dependent Spindle Positioning Pathway And
RESEARCH ARTICLE HMMR acts in the PLK1-dependent spindle positioning pathway and supports neural development Marisa Connell1†, Helen Chen1†, Jihong Jiang1, Chia-Wei Kuan2, Abbas Fotovati1, Tony LH Chu1, Zhengcheng He1, Tess C Lengyell3, Huaibiao Li4, Torsten Kroll4, Amanda M Li1, Daniel Goldowitz3,5, Lucien Frappart4, Aspasia Ploubidou4, Millan S Patel5, Linda M Pilarski6, Elizabeth M Simpson3,5, Philipp F Lange2,7, Douglas W Allan8, Christopher A Maxwell1,7* 1Department of Paediatrics, University of British Columbia, Vancouver, Canada; 2Department of Pathology and Laboratory Medicine, University of British Columbia, Vancouver, Canada; 3Centre for Molecular Medicine and Therapeutics, University of British Columbia, Vancouver, Canada; 4Leibniz Institute on Aging—Fritz Lipmann Institute, Beutenbergstrasse, Germany; 5Department of Medical Genetics, University of British Columbia, Vancouver, Canada; 6Cross Cancer Institute, Department of Oncology, University of Alberta, Edmonton, Canada; 7Michael Cuccione Childhood Cancer Research Program, BC Children’s Hospital, Vancouver, Canada; 8Department of Cellular and Physiological Sciences, Life Sciences Centre, University of British Columbia, Vancouver, Canada Abstract Oriented cell division is one mechanism progenitor cells use during development and to maintain tissue homeostasis. Common to most cell types is the asymmetric establishment and regulation of cortical NuMA-dynein complexes that position the mitotic spindle. Here, we discover *For correspondence: cmaxwell@ bcchr.ubc.ca that HMMR acts at centrosomes in a PLK1-dependent pathway that locates active Ran and modulates the cortical localization of NuMA-dynein complexes to correct mispositioned spindles. † These authors contributed This pathway was discovered through the creation and analysis of Hmmr-knockout mice, which equally to this work suffer neonatal lethality with defective neural development and pleiotropic phenotypes in multiple Competing interests: The tissues. -

Host Cell Factors Necessary for Influenza a Infection: Meta-Analysis of Genome Wide Studies
Host Cell Factors Necessary for Influenza A Infection: Meta-Analysis of Genome Wide Studies Juliana S. Capitanio and Richard W. Wozniak Department of Cell Biology, Faculty of Medicine and Dentistry, University of Alberta Abstract: The Influenza A virus belongs to the Orthomyxoviridae family. Influenza virus infection occurs yearly in all countries of the world. It usually kills between 250,000 and 500,000 people and causes severe illness in millions more. Over the last century alone we have seen 3 global influenza pandemics. The great human and financial cost of this disease has made it the second most studied virus today, behind HIV. Recently, several genome-wide RNA interference studies have focused on identifying host molecules that participate in Influen- za infection. We used nine of these studies for this meta-analysis. Even though the overlap among genes identified in multiple screens was small, network analysis indicates that similar protein complexes and biological functions of the host were present. As a result, several host gene complexes important for the Influenza virus life cycle were identified. The biological function and the relevance of each identified protein complex in the Influenza virus life cycle is further detailed in this paper. Background and PA bound to the viral genome via nucleoprotein (NP). The viral core is enveloped by a lipid membrane derived from Influenza virus the host cell. The viral protein M1 underlies the membrane and anchors NEP/NS2. Hemagglutinin (HA), neuraminidase Viruses are the simplest life form on earth. They parasite host (NA), and M2 proteins are inserted into the envelope, facing organisms and subvert the host cellular machinery for differ- the viral exterior. -

Supplemental Data Heidel Et Al
Supplemental data Heidel et al. Table of Contents 1. Sequencing strategy and statistics ...................................................................................................... 2 2. Genome structure ............................................................................................................................... 2 2.1 Extrachromosal elements .............................................................................................................. 2 2.2 Chromosome structure ................................................................................................................. 3 2.3 Repetitive elements ...................................................................................................................... 5 3. Coding sequences ................................................................................................................................ 5 3.1 Homopolymer tracts ..................................................................................................................... 5 3.2 Gene families and orthology relationships ................................................................................... 7 3.3 Synteny analysis .......................................................................................................................... 11 4. Protein functional domains ............................................................................................................... 12 5. Protein families ................................................................................................................................. -

Novel Gene Signatures for Stage Classification of the Squamous Cell
www.nature.com/scientificreports OPEN Novel gene signatures for stage classifcation of the squamous cell carcinoma of the lung Angel Juarez‑Flores, Gabriel S. Zamudio & Marco V. José* The squamous cell carcinoma of the lung (SCLC) is one of the most common types of lung cancer. As GLOBOCAN reported in 2018, lung cancer was the frst cause of death and new cases by cancer worldwide. Typically, diagnosis is made in the later stages of the disease with few treatment options available. The goal of this work was to fnd some key components underlying each stage of the disease, to help in the classifcation of tumor samples, and to increase the available options for experimental assays and molecular targets that could be used in treatment development. We employed two approaches. The frst was based in the classic method of diferential gene expression analysis, network analysis, and a novel concept known as network gatekeepers. The second approach was using machine learning algorithms. From our combined approach, we identifed two sets of genes that could function as a signature to identify each stage of the cancer pathology. We also arrived at a network of 55 nodes, which according to their biological functions, they can be regarded as drivers in this cancer. Although biological experiments are necessary for their validation, we proposed that all these genes could be used for cancer development treatments. As GLOBOCAN reported in 2018, lung cancer was the frst cause of deaths and new cases by cancer worldwide 1. Squamous cell carcinoma of the lung (SCC) is one type of lung cancer which comprises approximately 30% of all lung cancer cases. -
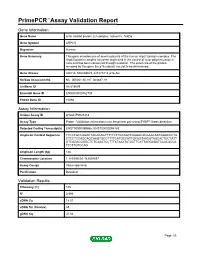
Primepcr™Assay Validation Report
PrimePCR™Assay Validation Report Gene Information Gene Name actin related protein 2/3 complex, subunit 5, 16kDa Gene Symbol ARPC5 Organism Human Gene Summary This gene encodes one of seven subunits of the human Arp2/3 protein complex. The Arp2/3 protein complex has been implicated in the control of actin polymerization in cells and has been conserved through evolution. The exact role of the protein encoded by this gene the p16 subunit has yet to be determined. Gene Aliases ARC16, MGC88523, dJ127C7.3, p16-Arc RefSeq Accession No. NC_000001.10, NT_004487.19 UniGene ID Hs.518609 Ensembl Gene ID ENSG00000162704 Entrez Gene ID 10092 Assay Information Unique Assay ID qHsaCIP0027218 Assay Type Probe - Validation information is for the primer pair using SYBR® Green detection Detected Coding Transcript(s) ENST00000359856, ENST00000294742 Amplicon Context Sequence TTCCTGCCAGACTACACAGTTTTTCTTGCAGTCAAGACACGAACAATGGACCCTA CTCCTCCAGCAGCAAGTGCCTTTTCATGCCATTGCAGTAACATAGCACTGCTATT GTCAGACGGGCTCTCAAATCCTTTATAAATATACTTCATTAGGAGATCCACACCA TTCTTGTCCAG Amplicon Length (bp) 146 Chromosome Location 1:183596656-183599697 Assay Design Intron-spanning Purification Desalted Validation Results Efficiency (%) 105 R2 0.996 cDNA Cq 18.01 cDNA Tm (Celsius) 83 gDNA Cq 37.04 Page 1/5 PrimePCR™Assay Validation Report Specificity (%) 100 Information to assist with data interpretation is provided at the end of this report. Page 2/5 PrimePCR™Assay Validation Report ARPC5, Human Amplification Plot Amplification of cDNA generated from 25 ng of universal reference RNA Melt Peak -

Chipenrich: a Package for Gene Set Enrichment Testing of Genome Region Data
chipenrich: A package for gene set enrichment testing of genome region data R.P. Welch, C. Lee, R.G. Cavalcante, R.A. Smith, P. Imbriano, S. Patil, T. Weymouth, L.J. Scott, M.A. Sartor October 13, 2015 Contents 1 Introduction 1 2 Synopsis 1 3 Locus definitions 3 4 Mappability 4 4.1 Base pair mappability . 4 4.2 Locus mappability . 4 5 Examples 4 5.1 Diagnostic plots . 4 5.2 ChIP-Enrich . 4 5.3 ChIP-Enrich with mappability . 9 5.4 Broad-Enrich . 9 5.5 Fisher's exact test . 10 6 Output 10 6.1 Peak-to-gene assignments . 11 6.2 Gene set enrichment test results . 11 7 References 12 1 Introduction This document describes how to use chipenrich to analyze results from ChIP-Seq experiments and other DNA sequencing experiments that result in a set of genomic regions. chipenrich includes two methods that adjust for potential confounders of gene set enrichment testing (locus length and mappability of the sequence reads). The first method chipenrich is designed for use with transcription-factor based ChIP-seq experiments and other DNA sequencing experiments with narrow genomic regions. The second method broadenrich is designed for use with histone modification based ChIP-seq experiments and other DNA sequencing experiments with broad genomic regions. 2 Synopsis After starting R, the package should be loaded using the following: > library(chipenrich) This will load chipenrich, the chipenrich.data package, as well as all other dependency packages. The main function for conducting all gene set enrichment testing is chipenrich(). The defaults for the chipenrich() function are 1 chipenrich(peaks, out_name = "chipenrich", out_path = getwd(), genome = "hg19", genesets = c('GOBP', 'GOCC', 'GOMF'), locusdef = "nearest_tss ", method = "chipenrich", fisher_alt = "two.sided", use_mappability = F, read_length = 24, genome_length = NULL, qc_plots = T,n_cores=1) The \peaks" option should be either a data frame or character vector representing the path to a file containing the peaks.