Cronobacter Spp. 의 오염, 제어, 검출에 관한 최신 연구동향
Total Page:16
File Type:pdf, Size:1020Kb
Load more
Recommended publications
-

Identification and Virulence of Enterobacter Sakazakii
Industr & ial od M o i F c r Rajani et al., J Food Ind Microbiol 2016, 2:1 f o o b l i Journal of o a l n DOI: 10.4172/2572-4134.1000108 o r g u y o J ISSN: 2572-4134 Food & Industrial Microbiology Research Article Open Access Identification and Virulence of Enterobacter sakazakii Rajani CSR, Chaudhary A, Swarna A and Puniya AK* Dairy Microbiology Division, ICAR-National Dairy Research Institute, Karnal 132001, India Abstract Enterobacter sakazakii (formerly known as Cronobacter sakazakii) is an opportunistic pathogen that causes necrotizing enterocolitis, bacteremia and meningitis, especially in neonates. This study was an attempt to isolate E. sakazakii from different food and environmental sources so as to establish its presence and possible source of transmission. For this, 93 samples (i.e., 37 from dairy and 56 from non-dairy) were collected using standard procedures of sampling. Out of these samples, 45 isolates (i.e., 14 from dairy and 31 from other samples) were taken further on the basis of growth on tryptic soy agar. On further screening on the basis of Gram staining, catalase and oxidase test, only 27 isolates were observed to be positive. The positive isolates were also subjected to PCR based identification using species specific primers. Overall, 11 isolates confirmed E.as sakazakii were also tested for virulent characteristics (i.e., hemolytic activity, haemagglutination test and DNase production) and all the isolates were found to be positive showing a potential threat of infection through food commodities. Keywords: Enterobacter sakazakii; Cronobacter; Virulence lactoferrin showed some effect by reducing the viability of C. -

CHAPTER 1: General Introduction and Aims 1.1 the Genus Cronobacter: an Introduction
Diversity and virulence of the genus Cronobacter revealed by multilocus sequence typing (MLST) and comparative genomic analysis Susan Manju Joseph A thesis submitted in partial fulfilment of the requirements of Nottingham Trent University for the degree of Doctor of Philosophy July 2013 Experimental work contained in this thesis is original research carried out by the author, unless otherwise stated, in the School of Science and Technology at the Nottingham Trent University. No material contained herein has been submitted for any other degree, or at any other institution. This work is the intellectual property of the author. You may copy up to 5% of this work for private study, or personal, non-commercial research. Any re-use of the information contained within this document should be fully referenced, quoting the author, title, university, degree level and pagination. Queries or requests for any other use, or if a more substantial copy is required, should be directed in the owner(s) of the Intellectual Property Rights. Susan Manju Joseph ACKNOWLEDGEMENTS I would like to express my immense gratitude to my supervisor Prof. Stephen Forsythe for having offered me the opportunity to work on this very exciting project and for having been a motivating and inspiring mentor as well as friend through every stage of this PhD. His constant encouragement and availability for frequent meetings have played a very key role in the progress of this research project. I would also like to thank my co-supervisors, Dr. Alan McNally and Prof. Graham Ball for all the useful advice, guidance and participation they provided during the course of this PhD study. -
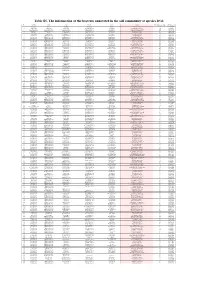
Table S5. the Information of the Bacteria Annotated in the Soil Community at Species Level
Table S5. The information of the bacteria annotated in the soil community at species level No. Phylum Class Order Family Genus Species The number of contigs Abundance(%) 1 Firmicutes Bacilli Bacillales Bacillaceae Bacillus Bacillus cereus 1749 5.145782459 2 Bacteroidetes Cytophagia Cytophagales Hymenobacteraceae Hymenobacter Hymenobacter sedentarius 1538 4.52499338 3 Gemmatimonadetes Gemmatimonadetes Gemmatimonadales Gemmatimonadaceae Gemmatirosa Gemmatirosa kalamazoonesis 1020 3.000970902 4 Proteobacteria Alphaproteobacteria Sphingomonadales Sphingomonadaceae Sphingomonas Sphingomonas indica 797 2.344876284 5 Firmicutes Bacilli Lactobacillales Streptococcaceae Lactococcus Lactococcus piscium 542 1.594633558 6 Actinobacteria Thermoleophilia Solirubrobacterales Conexibacteraceae Conexibacter Conexibacter woesei 471 1.385742446 7 Proteobacteria Alphaproteobacteria Sphingomonadales Sphingomonadaceae Sphingomonas Sphingomonas taxi 430 1.265115184 8 Proteobacteria Alphaproteobacteria Sphingomonadales Sphingomonadaceae Sphingomonas Sphingomonas wittichii 388 1.141545794 9 Proteobacteria Alphaproteobacteria Sphingomonadales Sphingomonadaceae Sphingomonas Sphingomonas sp. FARSPH 298 0.876754244 10 Proteobacteria Alphaproteobacteria Sphingomonadales Sphingomonadaceae Sphingomonas Sorangium cellulosum 260 0.764953367 11 Proteobacteria Deltaproteobacteria Myxococcales Polyangiaceae Sorangium Sphingomonas sp. Cra20 260 0.764953367 12 Proteobacteria Alphaproteobacteria Sphingomonadales Sphingomonadaceae Sphingomonas Sphingomonas panacis 252 0.741416341 -

Redalyc.Prevalence and Identification by Multiplex Polymerase Chain Reaction Patterns of Cronobacter Spp. Isolated from Plant
Ciência e Tecnologia de Alimentos ISSN: 0101-2061 [email protected] Sociedade Brasileira de Ciência e Tecnologia de Alimentos Brasil AKSU, Filiz; SANDIKÇI ALTUNATMAZ, Sema; ISSA, Ghassan; ÖZMEN TOGAY, Sine; AKSU, Harun Prevalence and identification by multiplex polymerase chain reaction patterns of Cronobacter spp. isolated from plant-based foods Ciência e Tecnologia de Alimentos, vol. 36, núm. 4, octubre-diciembre, 2016, pp. 730-736 Sociedade Brasileira de Ciência e Tecnologia de Alimentos Campinas, Brasil Available in: http://www.redalyc.org/articulo.oa?id=395949545024 How to cite Complete issue Scientific Information System More information about this article Network of Scientific Journals from Latin America, the Caribbean, Spain and Portugal Journal's homepage in redalyc.org Non-profit academic project, developed under the open access initiative a ISSN 0101-2061 Identification of Cronobacter isolated from foodstuff Food Science and Technology DDOI http://dx.doi.org/10.1590/1678-457X.16916 Prevalence and identification by multiplex polymerase chain reaction patterns of Cronobacter spp. isolated from plant-based foods Filiz AKSU1*, Sema SANDIKÇI ALTUNATMAZ1, Ghassan ISSA2, Sine ÖZMEN TOGAY3, Harun AKSU4 Abstract Cronobacter spp. involves a group of opportunistic pathogens that cause meningitis in newborns, immunosuppressed individuals with a mortality rate of 50-80%. Seven species like C. sakazakii, C. malonaticus, C. muytjensii, C. turicensis, C. dublinensis, C. universalis, C. condimenti are included in this genus which has been a subject of research especially in the bacteriologic analysis of baby foods. However, since these species were detected also in prepared foodstuffs. The objective of this study was to assert the presence of Cronobacter spp. -

Prevalence, Distribution, and Phylogeny of Type Two Toxin-Antitoxin Genes Possessed by Cronobacter Species Where C. Sakazakii Homologs Follow Sequence Type Lineages
microorganisms Article Prevalence, Distribution, and Phylogeny of Type Two Toxin-Antitoxin Genes Possessed by Cronobacter Species where C. sakazakii Homologs Follow Sequence Type Lineages Samantha Finkelstein, Flavia Negrete, Hyein Jang, Jayanthi Gangiredla, Mark Mammel, Isha R. Patel, Hannah R. Chase, JungHa Woo, YouYoung Lee, Caroline Z. Wang, Leah Weinstein, Ben D. Tall * and Gopal R. Gopinath Center of Food Safety and Applied Nutrition, U. S. Food and Drug Administration, 8301 MuirKirk Rd, Laurel, MD 20708, USA; sfi[email protected] (S.F.); [email protected] (F.N.); [email protected] (H.J.); [email protected] (J.G.); [email protected] (M.M.); [email protected] (I.R.P.); [email protected] (H.R.C.); [email protected] (J.W.); [email protected] (Y.L.); [email protected] (C.Z.W.); [email protected] (L.W.); [email protected] (G.R.G.) * Correspondence: [email protected] Received: 4 October 2019; Accepted: 9 November 2019; Published: 12 November 2019 Abstract: Cronobacter species are a group of foodborne pathogenic bacteria that cause both intestinal and systemic human disease in individuals of all age groups. Little is known about the mechanisms that Cronobacter employ to survive and persist in foods and other environments. Toxin–antitoxin (TA) genes are thought to play a role in bacterial stress physiology, as well as in the stabilization of horizontally-acquired re-combinatorial elements such as plasmids, phage, and transposons. TA systems have been implicated in the formation of a persistence phenotype in some bacterial species including Escherichia coli and Salmonella. -

Biocontrol of Cronobacter Spp. Using Bacteriophage in Infant Formula
i Biocontrol of Cronobacter spp. using Bacteriophage in Infant Formula by Reza Abbasifar A Thesis presented to The University of Guelph In partial fulfillment of requirements for the degree of Doctor of Philosophy in Food Science Guelph, Ontario, Canada © Reza Abbasifar, May, 2013 ii ABSTRACT Biocontrol of Cronobacter spp. using Bacteriophage in Infant Formula Reza Abbasifar Advisor: Dr. Mansel W. Griffiths University of Guelph, 2013 Co-Advisor: Dr. Parviz M. Sabour The purpose of this research was to explore the potential application of lytic phages to control Cronobacter spp. in infant formula. More than two hundred and fifty phages were isolated from various environmental samples against different strains of Cronobacter spp. Selected phages were characterized by morphology, host range, and cross infectivity. The genomes of five novel Cronobacter phages [vB_CsaM_GAP31 (GAP31), vB_CsaM_GAP32 (GAP32), vB_CsaP_GAP52 (GAP52), vB_CsaM_GAP161 (GAP161), vB_CsaP_GAP227 (GAP227)] were sequenced. Phage GAP32 possess the second largest phage genome sequenced to date, and it is proposed that GAP32 belongs to a new genus of “Gap32likeviruses”. Phages GAP52 and GAP227 are the first C. sakazakii podoviruses whose genomes have been sequenced. None of the sequenced genomes showed homology to virulent or lysogenic genes. In addition, in vivo administration of phage GAP161 in the hemolymph of Galleria mellonella larvae showed no negative effects on the wellbeing of the larvae and could effectively prevent Cronobacter infection in the larvae. A cocktail of five phages was highly effective for biocontrol of three Cronobacter sakazakii strains present as a mixed culture in both broth media and contaminated reconstituted infant formula. This phage cocktail could be iii potentially used to control C. -

International Journal of Systematic and Evolutionary Microbiology (2016), 66, 5575–5599 DOI 10.1099/Ijsem.0.001485
International Journal of Systematic and Evolutionary Microbiology (2016), 66, 5575–5599 DOI 10.1099/ijsem.0.001485 Genome-based phylogeny and taxonomy of the ‘Enterobacteriales’: proposal for Enterobacterales ord. nov. divided into the families Enterobacteriaceae, Erwiniaceae fam. nov., Pectobacteriaceae fam. nov., Yersiniaceae fam. nov., Hafniaceae fam. nov., Morganellaceae fam. nov., and Budviciaceae fam. nov. Mobolaji Adeolu,† Seema Alnajar,† Sohail Naushad and Radhey S. Gupta Correspondence Department of Biochemistry and Biomedical Sciences, McMaster University, Hamilton, Ontario, Radhey S. Gupta L8N 3Z5, Canada [email protected] Understanding of the phylogeny and interrelationships of the genera within the order ‘Enterobacteriales’ has proven difficult using the 16S rRNA gene and other single-gene or limited multi-gene approaches. In this work, we have completed comprehensive comparative genomic analyses of the members of the order ‘Enterobacteriales’ which includes phylogenetic reconstructions based on 1548 core proteins, 53 ribosomal proteins and four multilocus sequence analysis proteins, as well as examining the overall genome similarity amongst the members of this order. The results of these analyses all support the existence of seven distinct monophyletic groups of genera within the order ‘Enterobacteriales’. In parallel, our analyses of protein sequences from the ‘Enterobacteriales’ genomes have identified numerous molecular characteristics in the forms of conserved signature insertions/deletions, which are specifically shared by the members of the identified clades and independently support their monophyly and distinctness. Many of these groupings, either in part or in whole, have been recognized in previous evolutionary studies, but have not been consistently resolved as monophyletic entities in 16S rRNA gene trees. The work presented here represents the first comprehensive, genome- scale taxonomic analysis of the entirety of the order ‘Enterobacteriales’. -

Evidence for a Direct Link Between the Tol-Pal Protein Complex and Gram Negative Bacteria Cell Division Via an Interaction Between Tolq and the Divisome Protein Ftsn
EVIDENCE FOR A DIRECT LINK BETWEEN THE TOL-PAL PROTEIN COMPLEX AND GRAM NEGATIVE BACTERIA CELL DIVISION VIA AN INTERACTION BETWEEN TOLQ AND THE DIVISOME PROTEIN FTSN Mary A. Teleha A Dissertation Submitted to the Graduate College of Bowling Green State University in partial fulfillment of the requirements for the degree of DOCTOR OF PHILOSOPHY August 2013 Committee: Dr. Ray A. Larsen, Advisor Dr. Roudabeh J. Jamasbi Graduate Faculty Representative Dr. Rex L. Lowe Dr. Adam C. Miller Dr. Vipaporn Phuntumart Dr. Scott O. Rogers ii ABSTRACT Ray Larsen, Advisor The TolQ protein functions to couple cytoplasmic membrane-derived energy to support outer membrane processes in Gram negative bacteria. With other products of the widely-conserved tol-pal gene cluster, TolQ has been linked to the process of bacterial cell division. When present in excess, TolQ disrupts cell division, leading to filamentous growth of Escherichia coli. The potential role of TolQ in Gram negative cell division was investigated by a number of methods, including growth assays and immunoblot, two-hybrid, and mutational analyses. This filamentation phenotype is specific for TolQ over-expression independent of TolA and TolR levels, with the degree of filamentation directly proportional to TolQ levels. Over-expression of E. coli TolQ in closely related species indicates that this property of TolQ is not E. coli specific, as excess TolQ leads to a comparable phenotype in other Gram negatives. Bacterial two-hybrid analysis indicates a potential in vivo interaction between TolQ and the divisome protein FtsN, ostensibly one that competitively diverts FtsN from functioning efficiently during late-stage cell division. -

Phage S144, a New Polyvalent Phage Infecting Salmonella Spp. and Cronobacter Sakazakii
International Journal of Molecular Sciences Article Phage S144, a New Polyvalent Phage Infecting Salmonella spp. and Cronobacter sakazakii Michela Gambino 1 , Anders Nørgaard Sørensen 1 , Stephen Ahern 1 , Georgios Smyrlis 1, Yilmaz Emre Gencay 1 , Hanne Hendrix 2, Horst Neve 3 , Jean-Paul Noben 4 , Rob Lavigne 2 and Lone Brøndsted 1,* 1 Department of Veterinary and Animal Sciences, University of Copenhagen, 1870 Frederiksberg C, Denmark; [email protected] (M.G.); [email protected] (A.N.S.); [email protected] (S.A.); [email protected] (G.S.); [email protected] (Y.E.G.) 2 Laboratory of Gene Technology, KU Leuven, 3001 Leuven, Belgium; [email protected] (H.H.); [email protected] (R.L.) 3 Department of Microbiology and Biotechnology, Max Rubner-Institut, Federal Research Institute of Nutrition and Food, 24103 Kiel, Germany; [email protected] 4 Biomedical Research Institute and Transnational University Limburg, Hasselt University, BE3590 Diepenbeek, Belgium; [email protected] * Correspondence: [email protected] Received: 25 June 2020; Accepted: 21 July 2020; Published: 22 July 2020 Abstract: Phages are generally considered species- or even strain-specific, yet polyvalent phages are able to infect bacteria from different genera. Here, we characterize the novel polyvalent phage S144, a member of the Loughboroughvirus genus. By screening 211 Enterobacteriaceae strains, we found that phage S144 forms plaques on specific serovars of Salmonella enterica subsp. enterica and on Cronobacter sakazakii. Analysis of phage resistant mutants suggests that the O-antigen of lipopolysaccharide is the phage receptor in both bacterial genera. The S144 genome consists of 53,628 bp and encodes 80 open reading frames (ORFs), but no tRNA genes. -

Enterobacter Sakazakii)
J. Microbiol. Biotechnol. (2011), 21(5), 509–514 doi: 10.4014/jmb.1007.07059 First published online 3 March 2011 The Phenotypic and Genotypic Characterization of Korean Isolates of Cronobacter spp. (Enterobacter sakazakii) Kim, Jung-Beom1, Suk-Ho Kang1, Yong-Bae Park1, Jae-Ho Choi2, Sung-Jin Park2,3, Seung-Hak Cho4, Mi-Sun Park4, Hae Kyung Lee5, Na-Jung Choi2, Ha-Na Kim2, and Deog-Hwan Oh2* 1Division of Health Research and Planning, Gyeonggi-do Research Institute of Health and Environment, Suwon 440-290, Korea 2School of Bioscience and Biotechnology, Kangwon National University, Chuncheon 200-701, Korea 3Center of Senior Industry, Youngdong University, Youngdong-gun, Chungbuk 370-701, Korea 4Division of Enteric Bacterial Infections, Center for Infectious Diseases, National Institute of Health, Seoul 122-701, Korea 5Department of Laboratory Medicine, Catholic University College of Medicine, Uijongbu 480-130, Korea Received: July 30, 2010 / Revised: February 8, 2011 / Accepted: February 11, 2011 This study was conducted to investigate the phenotypic and was initially known as yellow-pigmented Enterobacter genotypic characteristics of Korean isolates of Cronobacter cloacae and reclassified based on biochemical characteristics, spp. (Enterobacter sakazakii). A total of 43 Cronobacter DNA-DNA hybridization, and antibiotic susceptibility spp., including 5 clinical isolates, 34 food isolates, 2 patterns in 1980 [5, 18]. Cronobacter spp. infection, which environmental isolates, and 2 reference strains (C. sakazakii causes life-threatening meningitis, septicemia, and necrotizing ATCC 29004 and C. muytjensii ATCC51329) were used in enterocolitis in infants, has been implicated in foodborne this study. Korean isolates of Cronobacter spp. were outbreaks worldwide [17, 22]. The pathogen has been divided into 11 biogroups according to their biochemical isolated from a variety of food, clinical, and environmental profiles and 3 genomic groups based on the analysis of sources including cheese, vegetables, grains, soil, and powdered their 16S rRNA gene sequences. -

Cronobacter: an Emerging Opportunistic Pathogen Associated with Neonatal Meningitis, Sepsis and Necrotizing Enterocolitis
Journal of Perinatology (2013) 33, 581–585 & 2013 Nature America, Inc. All rights reserved 0743-8346/13 www.nature.com/jp STATE-OF-THE-ART Cronobacter: an emerging opportunistic pathogen associated with neonatal meningitis, sepsis and necrotizing enterocolitis CJ Hunter1,2 and JF Bean1 Members of the genus Cronobacter are an emerging group of opportunist Gram-negative pathogens. This genus was previously thought to be a single species, called Enterobacter sakazakii. Cronobacter spp. typically affect low-birth-weight neonates, causing life-threatening meningitis, sepsis and necrotizing enterocolitis. Outbreaks of disease have been associated with contaminated infant formula, although the primary environmental source remains elusive. Advanced understanding of these bacteria and better classification has been obtained by improved detection techniques and genomic analysis. Research has begun to characterize the virulence factors and pathogenic potential of Cronobacter. Investigations into sterilization techniques and protocols for minimizing the risk of contamination have been reviewed at national and international forums. In this review, we explore the clinical impact of Cronobacter neonatal and pediatric infections, discuss virulence and pathogenesis, and review prevention and treatment strategies. Journal of Perinatology (2013) 33, 581–585; doi:10.1038/jp.2013.26; published online 28 March 2013 Keywords: Cronobacter sakazakii; meningitis; necrotizing enterocolitis; neonatal infections; infant formula INTRODUCTION single clinical setting.10 Cronobacter neonatal infection rates Cronobacter is an emerging genus of opportunistic Gram-negative remain low and are reported in the USA as one Cronobacter pathogens associated with potentially fatal neonatal infections, infection per 100 000 infants, 8.7 per 100 000 low-birth-weight including meningitis, sepsis and necrotizing enterocolitis (NEC).1 neonates, and one Cronobacter infection per 10 660 very low- 13 These infections typically affect our smallest and most vulnerable birth-weight neonates. -

Isolation of Cronobacter Spp.(Formerly Enterobacter Sakazakii) from Infant
BMC Microbiology BioMed Central Research article Open Access Isolation of Cronobacter spp. (formerly Enterobacter sakazakii) from infant food, herbs and environmental samples and the subsequent identification and confirmation of the isolates using biochemical, chromogenic assays, PCR and 16S rRNA sequencing Ziad W Jaradat*†, Qotaiba O Ababneh†, Ismail M Saadoun, Nawal A Samara and Abrar M Rashdan Address: Department of Biotechnology and Genetic Engineering, Jordan University of Science and Technology, P. O. Box 3030, Irbid-22110, Jordan Email: Ziad W Jaradat* - [email protected]; Qotaiba O Ababneh - [email protected]; Ismail M Saadoun - [email protected]; Nawal A Samara - [email protected]; Abrar M Rashdan - [email protected] * Corresponding author †Equal contributors Published: 27 October 2009 Received: 10 March 2009 Accepted: 27 October 2009 BMC Microbiology 2009, 9:225 doi:10.1186/1471-2180-9-225 This article is available from: http://www.biomedcentral.com/1471-2180/9/225 © 2009 Jaradat et al; licensee BioMed Central Ltd. This is an Open Access article distributed under the terms of the Creative Commons Attribution License (http://creativecommons.org/licenses/by/2.0), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited. Abstract Background: Cronobacter spp. (formerly Enterobacter sakazakii), are a group of Gram-negative pathogens that have been implicated as causative agents of meningitis and necrotizing enterocolitis in infants. The pathogens are linked to infant formula; however, they have also been isolated from a wide range of foods and environmental samples. Results: In this study, 233 samples of food, infant formula and environment were screened for the presence of Cronobacter spp.