WO 2007/000214 Al
Total Page:16
File Type:pdf, Size:1020Kb
Load more
Recommended publications
-

Piedra Blanca Trail Middle Sespe Creek/Pine Mountain Ridge, Ventura County, California by David L
Vascular Plants of the Piedra Blanca Trail Middle Sespe Creek/Pine Mountain Ridge, Ventura County, California By David L. Magney Botanical Name Common Name Habit Family Acer macrophyllum Bigleaf Maple T Sapindaceae Acmispon ? Lotus AH Fabaceae Acmispon glaber var. glaber Deerweed S Fabaceae Acmispon strigosus var. strigosus Strigose Lotus AH Fabaceae Acourtia microcephala Sacapellote PH Asteraceae Adenostoma fasciculatum Chamise S Rosaceae Agoseris ? Mountain Dandelion PH Asteraceae Alnus rhombifolia White Alder T Betulaceae Amorpha californica False Indigo S Fabaceae Antirrhinum multiflorum Sticky Snapdragon S Veronicaceae Aquilegia formosa Columbine PH Ranunculaceae Arctostaphylos glauca Bigberry Manzanita S Ericaceae Artemisia douglasiana Mugwort S Asteraceae Artemisia tridentata ssp. tridentata Great Basin Sagebrush S Asteraceae Asclepias eriocarpa Woolly Milkweed AH Apocynaceae Astragalus ? Milkvetch AH Fabaceae Avena barbata* Slender Wild Oat AG Poaceae Baccharis salicifolia Mulefat S Asteraceae Boechera arcuata Few-flowered Rock Cress PH Brassicaceae Brickellia californica California Brickellbush S Asteraceae Bromus ? Brome PG Poaceae Bromus madritensis ssp. rubens* Red Brome AG Poaceae Bromus tectorum var. tectorum* Downy Brome AG Poaceae Calocedrus decurrens Incense-cedar T Cupressaceae Calyptridium monandrum Common Calyptridium AH Montiaceae Calystegia malacophylla ssp. cf pedicellata Sierra Morning-glory PH Convolvulaceae Camissonia boothii ssp. decorticans Shreading Evening Primrose AH Onagraceae Camissonia campestris ssp. campestris? Mojave Sun-cup AH Onagraceae Camissoniopsis micrantha Tiny Primrose AH Onagraceae Camissoniopsis pallida ssp. pallida Pale Primrose AH Onagraceae Carex ? Sedge PG Cyperaceae Carex senta Rough Sedge PG Cyperaceae Castilleja ? Indian Paintbrush PH Orobanchaceae Castilleja affinis ssp. affinis Lay-and-Collie's Indian Paintbrush PH Orobanchaceae Castilleja foliolosa Woolly Indian Paintbrush PH Orobanchaceae Castilleja subinclusa ssp. subinclusa Long-leaved Indian Paintbrush PH Orobanchaceae Caulanthus coulteri var. -

Conserving Europe's Threatened Plants
Conserving Europe’s threatened plants Progress towards Target 8 of the Global Strategy for Plant Conservation Conserving Europe’s threatened plants Progress towards Target 8 of the Global Strategy for Plant Conservation By Suzanne Sharrock and Meirion Jones May 2009 Recommended citation: Sharrock, S. and Jones, M., 2009. Conserving Europe’s threatened plants: Progress towards Target 8 of the Global Strategy for Plant Conservation Botanic Gardens Conservation International, Richmond, UK ISBN 978-1-905164-30-1 Published by Botanic Gardens Conservation International Descanso House, 199 Kew Road, Richmond, Surrey, TW9 3BW, UK Design: John Morgan, [email protected] Acknowledgements The work of establishing a consolidated list of threatened Photo credits European plants was first initiated by Hugh Synge who developed the original database on which this report is based. All images are credited to BGCI with the exceptions of: We are most grateful to Hugh for providing this database to page 5, Nikos Krigas; page 8. Christophe Libert; page 10, BGCI and advising on further development of the list. The Pawel Kos; page 12 (upper), Nikos Krigas; page 14: James exacting task of inputting data from national Red Lists was Hitchmough; page 16 (lower), Jože Bavcon; page 17 (upper), carried out by Chris Cockel and without his dedicated work, the Nkos Krigas; page 20 (upper), Anca Sarbu; page 21, Nikos list would not have been completed. Thank you for your efforts Krigas; page 22 (upper) Simon Williams; page 22 (lower), RBG Chris. We are grateful to all the members of the European Kew; page 23 (upper), Jo Packet; page 23 (lower), Sandrine Botanic Gardens Consortium and other colleagues from Europe Godefroid; page 24 (upper) Jože Bavcon; page 24 (lower), Frank who provided essential advice, guidance and supplementary Scumacher; page 25 (upper) Michael Burkart; page 25, (lower) information on the species included in the database. -

Botanical Name: LEAFY PLANT
LEAFY PLANT LIST Botanical Name: Common Name: Abelia 'Edward Goucher' Glossy Pink Abelia Abutilon palmeri Indian Mallow Acacia aneura Mulga Acacia constricta White-Thorn Acacia Acacia craspedocarpa Leatherleaf Acacia Acacia farnesiana (smallii) Sweet Acacia Acacia greggii Cat-Claw Acacia Acacia redolens Desert Carpet Acacia Acacia rigidula Blackbrush Acacia Acacia salicina Willow Acacia Acacia species Fern Acacia Acacia willardiana Palo Blanco Acacia Acalpha monostachya Raspberry Fuzzies Agastache pallidaflora Giant Pale Hyssop Ageratum corymbosum Blue Butterfly Mist Ageratum houstonianum Blue Floss Flower Ageratum species Blue Ageratum Aloysia gratissima Bee Bush Aloysia wrightii Wright's Bee Bush Ambrosia deltoidea Bursage Anemopsis californica Yerba Mansa Anisacanthus quadrifidus Flame Bush Anisacanthus thurberi Desert Honeysuckle Antiginon leptopus Queen's Wreath Vine Aquilegia chrysantha Golden Colmbine Aristida purpurea Purple Three Awn Grass Artemisia filifolia Sand Sage Artemisia frigida Fringed Sage Artemisia X 'Powis Castle' Powis Castle Wormwood Asclepias angustifolia Arizona Milkweed Asclepias curassavica Blood Flower Asclepias curassavica X 'Sunshine' Yellow Bloodflower Asclepias linearis Pineleaf Milkweed Asclepias subulata Desert Milkweed Asclepias tuberosa Butterfly Weed Atriplex canescens Four Wing Saltbush Atriplex lentiformis Quailbush Baileya multiradiata Desert Marigold Bauhinia lunarioides Orchid Tree Berlandiera lyrata Chocolate Flower Bignonia capreolata Crossvine Bougainvillea Sp. Bougainvillea Bouteloua gracilis -

Guide to Native Plants
- AA GUIDEGUIDE TOTO THETHE NATIVENATIVE PLANTS,PLANTS, NATURALNATURAL PLANTPLANT COMMUNITIESCOMMUNITIES ANDAND THETHE EXOTICEXOTIC ANDAND INVASIVEINVASIVE SPECIESSPECIES OFOF EASTEAST HAMPTONHAMPTON TOWNTOWN EAST HAMPTON TOWN Natural Resources Department TableTable ofof Contents:Contents: Spotted Beebalm (Monarda punctata) Narrative: Pages 1-17 Quick Reference Max Clearing Table: Page 18 Map: East Hampton Native Plant Habitats Map TABS: East Hampton Plant Habitats (1-12); Wetlands flora (13-15): 1. Outer Dunes Plant Spacing 2. Bay Bluffs 3. Amagansett Inner Dunes (AID) 4. Tidal Marsh (TM) Table: A 5. Montauk Mesic Forest (MMF) 6. Montauk Moorland (MM) guideline for the 7. North of Moraine Coastal Deciduous (NMCD) 8. Morainal Deciduous (MD) 9. Pine Barrens or Pitch Pine Oak Forest (PB) (PPO) number of 10. Montauk Grasslands (MG) 11. Northwest Woods (NWW) plants needed 12. Old Fields 13. Freshwater Wetlands 14. Brackish Wetlands and Buffer for an area: 15. East Hampton Wetland Flora by Type Page 19 Native Plants-Resistance to Deer Damage: Pages 20-21 Local Native Plant Landscapers, Arborists, Native Plant Growers and Suppliers: Pages 22-23 Exotic and Invasive Species: Pages 24-33 Native Wildflower Pictures: Pages 34-45 Samdplain Gerardia (Agalinas acuta) Introduction to our native landscape What is a native plant? Native plants are plants that are indigenous to a particular area or region. In North America we are referring to the flora that existed in an area or region before European settlement. Native plants occur within specific plant communities that vary in species composition depending on the habitat in which they are found. A few examples of habitats are tidal wetlands, woodlands, meadows and dunelands. -

Harbor Regional Park “Dirty Dozen” Weeds Identification
To Protect and Preserve Natural Habitat HARBOR REGIONAL PARK “DIRTY DOZEN” WEEDS IDENTIFICATION THIS BOOKLET WAS CREATED TO ASSIST DEPARTMENT OF RECREATION AND PARK STAFF AND VOLUNTEERS IN THE IDENTIFICATION OF PROBLEMATIC WEEDS. THE NAME “DIRTY DOZEN” WAS GIVEN TO THE TWELVE PLANTS THAT PREVENT THE ESTABLISHMENT OF NATIVE FLORA DUE TO THEIR HIGH REPRODUCTIVE RATE AND ACCELERATED GROWTH. THE “DIRTY DOZEN” ARE IDENTIFIED, ILLUSTRATED, AND LISTED IN THE ORDER THAT ADVERSELY AFFECT THE NATURAL ECOSYSTEM OF HARBOR REGIONAL PARK. 2 MAIN GOALS AND OBJECTIVES OF THIS BOOKLET 1) Support and restore the natural ecosystem found in Harbor Regional Park through the management and control of invasive plants. 2) To establish an Integrated Pest Management Program specific to Harbor Regional Park. 3) Build valuable resources for Department of Recreation and Parks staff and the public. 3 Some exotic plants, as well as native vegetation, with aggressive qualities may be considered a weed if it adversely affect the sustainability of the natural areas and encroaches into developed landscapes. Weed problems can be largely avoided by careful landscape design, soil preparation before planting, and adequately scheduled irrigation and mulching. Weed control can be achieved through a combination of the following five control methods: PREVENTIVE: Preventive method is defined as keeping the weeds from entering or becoming established in the area. Monitoring the area for early detection of unwanted plants is crucial for the preventative methods to work. If a new weed is discovered, immediate actions need to be taken in order to prevent seed production and establishment. CULTURAL: Cultural method is defined as maintenance practices that will make it difficult for weeds to grow or become established, (i.e., select proper plants for the location, irrigation management, and pruning). -
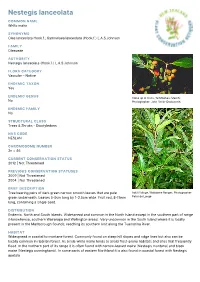
Nestegis Lanceolata
Nestegis lanceolata COMMON NAME White maire SYNONYMS Olea lanceolata Hook.f.; Gymnelaea lanceolata (Hook.f.) L.A.S.Johnson FAMILY Oleaceae AUTHORITY Nestegis lanceolata (Hook.f.) L.A.S.Johnson FLORA CATEGORY Vascular – Native ENDEMIC TAXON Yes ENDEMIC GENUS Close up of fruits, Te Moehau (March). No Photographer: John Smith-Dodsworth ENDEMIC FAMILY No STRUCTURAL CLASS Trees & Shrubs - Dicotyledons NVS CODE NESLAN CHROMOSOME NUMBER 2n = 46 CURRENT CONSERVATION STATUS 2012 | Not Threatened PREVIOUS CONSERVATION STATUSES 2009 | Not Threatened 2004 | Not Threatened BRIEF DESCRIPTION Tree bearing pairs of dark green narrow smooth leaves that are pale Adult foliage, Waitakere Ranges. Photographer: green underneath. Leaves 5-9cm long by 1-2.5cm wide. Fruit red, 8-11mm Peter de Lange long, containing a single seed. DISTRIBUTION Endemic. North and South Islands. Widespread and common in the North Island except in the southern part of range (Horowhenua, southern Wairarapa and Wellington areas). Very uncommon in the South Island where it is locally present in the Marlborough Sounds, reaching its southern limit along the Tuamarina River. HABITAT Widespread in coastal to montane forest. Commonly found on steep hill slopes and ridge lines but also can be locally common in riparian forest. As a rule white maire tends to avoid frost-prone habitats and sites that frequently flood. In the northern part of its range it is often found with narrow-leaved maire (Nestegis montana) and black maire (Nestegis cunninghamii). In some parts of eastern Northland it is also found in coastal forest with Nestegis apetala. FEATURES Stout gynodioecious spreading tree up to 20 m tall usually forming a domed canopy; trunk up to c. -

Chionanthus (Oleaceae) (Stapf) Kiew, Comb. Sagu, Padang Unique Among Being Ridged. Its Strongly Flattened Twigs, Long Petioles
BLUMEA 43 (1998) 471-477 Name changes for Malesian species of Chionanthus (Oleaceae) Ruth Kiew Singapore Botanic Gardens, Cluny Road, Singapore 259569 Summary New combinations under Chionanthus L. are made for Linociera beccarii, L. brassii, L. clementis, L. gigas, L. hahlii, L. kajewskii, L. nitida, L. remotinervia, L. riparia, L. rupicola, L. salicifolia, L. and L. Linociera is with C. L. sessiliflora stenura. cumingiana synonymous ramiflorus, novo- guineensis and L. ovalis with C. rupicolus, L. papuasica with C. sessiliflorus and L. pubipanicu- be lata with C. mala-elengi subsp. terniflorus. Linociera macrophylla sensu Whitmore proves to C. hahlii. Key words '. Malesia, Chionanthus,Oleaceae. Introduction The reduction of Linociera Sw. to Chionanthus L. (Steam, 1976) necessitates name changes to be made for species described inLinociera. In addition, as the family has been studied on a geographical rather than country basis, several species prove to be In for Vidal and two synonyms. some cases, notably a type Ledermanntypes, neotypes have had to be chosen because the holotype is no longer extant and isotypes have not been located. 1. Chionanthus beccarii (Stapf) Kiew, comb. nov. Linociera beccarii Stapf, Kew Bull. (1915) 115. —Type: Beccari PS 826 (holoK; isoL), Sumatra, Padang, Ayer Mancior. Distribution — Malesia: Sumatra (G. Leuser, G. Sagu, Padang and Asahan). — rather it is from Note Apparently a rare tree, known only the northern half of Sumatrawhere it grows in mountainforest between 360 and 1200 m. Its large fruit is unique among Malesian Chionanthus in being flattened laterally as well as being ridged. Its strongly flattened twigs, long petioles, narrowly obovate leaves with an acute apex, and rotund foliaceous bracts combine to make it a distinctive species. -

Vegetable Gardening Vegetable Gardening
TheThe AmericanAmerican GARDENERGARDENER® The Magazine of the American Horticultural Society January / February 2009 Vegetable Gardening tips for success New Plants and TTrendsrends for 2009 How to Prune Deciduous Shrubs Sweet Rewards of Indoor Citrus Confidence shows. Because a mistake can ruin an entire gardening season, passionate gardeners don’t like to take chances. That’s why there’s Osmocote® Smart-Release® Plant Food. It’s guaranteed not to burn when used as directed, and the granules don’t easily wash away, no matter how much you water. Better still, Osmocote feeds plants continuously and consistently for four full months, so you can garden with confidence. Maybe that’s why passionate gardeners have trusted Osmocote for 40 years. Looking for expert advice and answers to your gardening questions? Visit PlantersPlace.com — a fresh, new online gardening community. © 2007, Scotts-Sierra Horticulture Products Company. World rights reserved. www.osmocote.com contents Volume 88, Number 1 . January / February 2009 FEATURES DEPARTMENTS 5 NOTES FROM RIVER FARM 6 MEMBERS’ FORUM 8 NEWS FROM AHS Renee’s Garden sponsors 2009 Seed Exchange, Stanley Smith Horticultural Trust grant funds future library at River Farm, AHS welcomes new members to Board of Directors, save the date for the 17th annual National Children & Youth Garden Symposium in July. 42 ONE ON ONE WITH… Bonnie Harper-Lore, America’s roadside ecologist. page 14 44 GARDENER’S NOTEBOOK All-America Selections winners for 2009, scientists discover new plant hormone, NEW PLANTS AND TRENDS FOR 2009 BY DOREEN G. HOWARD 14 Massachusetts Horticultural Society forced Get a sneak peek at some of the exciting plants that will hit the to cancel one of market this year, along with expert insight on garden trends. -

Approved Plant Palette: Horseshoe Canyon
Section Twelve HORSESHOE CANYON HORSESHOE CANYON APPROVED PLANT LIST Zone Legend N = Native Nt = Native Transition S = Semi-Private P = Private TREES Botanical Name Common Name Zones Acacia abyssinica Abyssinian Acacia S,P Acacia aneura Mulga S,P Acacia berlandieri Berlandier Acacia S,P Acacia constricta Whitethorn Acacia S,P Acacia greggii Catclaw Acacia N,Nt,S,P Acacia pendula Pendulous Acacia S,P Acacia roemeriana Roemer Acacia S,P Acacia saligna Blue-Leaf Wattle S,P Acacia schaffneri Twisted Acacia S,P Acacia smallii (farnesiana) Sweet Acacia Nt,S,P Acacia willardiana Palo Blanco Nt,S,P Bauhinia congesta Anacacho Orchid Tree S,P Caesalpinia cacalaco Cascalote S,P Caesalpinia mexicana Mexican Bird of Paradise Nt,S,P Canotia holacantha Crucifi xion Thorn N,Nt,S,P Cercidium ‘Desert Museum’ Hybrid Palo Verde S,P Cercidium fl oridum Blue Palo Verde N,Nt,S,P Cercidium microphyllum Foothills Palo Verde N,Nt,S,P Cercis canadensis v. mexicana Mexican Redbud S,P Chilopsis linearis Desert Willow Nt,S,P Cordia boissieri Anacahuita S,P Forestiera neomexicana Desert Olive S,P Fraxinus greggii Littleleaf Ash P Leucaena retusa Golden Ball Lead Tree S,P Lysiloma microphylla v. thornberi Desert Fern Nt,S,P Olneya tesota Ironwood N,Nt,S,P Pithecellobium fl exicaule Texas Ebony S,P Pithecellobium mexicanum Mexican Ebony Nt,S,P Prosopis alba Argentine Mesquite S,P Prosopis chilensis Chilean Mesquite S,P Prosopis glandulosa v. glandulosa Texas Honey Mesquite Nt,S,P Prosopis pubescens Screwbean Mesquite Nt,S,P Prosopis velutina Velvet Mesquite N,Nt,S,P Quercus gambelii Gambel Oak P Robinia neomexicana New Mexico Locust S,P Sophora secundifl ora Texas Mountain Laurel S,P Ungnadia speciosa Mexican Buckeye S,P Vitex angus-castus Chaste Tree S,P The Horseshoe Canyon Approved Plant List is subject to change without notification. -

SGAP Cairns Newsletter
SGAP Cairns Newsletter May 2018 Newsletter 179 Editor’s Note Society for Growing Australian Plants, Inc. Cairns Branch. www.sgapcairns.org.au You may have noticed this month’s newsletter is not as [email protected] “flashy” or to the standard we have come to expect each month from our newsletter editor, Stuart, that is because 2018 -2019 Committee he is taking a well earned holiday! However, what we President: Tony Roberts lack in pizzazz we have made up in content! Don has Vice President: Pauline Lawie kindly put together a report on our trip to Ella Bay (which Secretary: Sandy Perkins ([email protected]) was a great day out, btw) and the plant of the month Treasurer: Val Carnie Newsletter: including an interesting google translation. And of Stuart Worboys course, there are the details on our next excursion to ([email protected]) Emerald Creek Falls. Looking forward to seeing you all Webmaster: Tony Roberts in May. Sandy Perkins Excursion Report ELLA BAY (HEATH POINT ) Sunday 15 April 2018 By Don Lawie The beach and dune walk planned for 11 March was cancelled due to heavy rain, local flooding and road washouts. Indeed, damage to Ella Bay Road was so bad that it was closed at Heath Point, the southern arm of Ella Bay, when we arrived on 15 April. Nothing daunted, we set off along the beach but were soon blocked by sharp volcanic rocks so diverted to the road and walked up a steep hill then returned to the beach beyond the rock barrier. The aim of the day was to discover what plants – trees, shrubs, vines etc.- grew in the area with fruits that would conceivably be eaten by shipwrecked mariners who were not knowledgeable about their edibility or otherwise. -

Plant Met Verstand En Vergeet Hem Niet! Essen, Deel 2
Plant met verstand en vergeet hem niet! Essen, deel 2 Op soortniveau zijn vooral de Gewone es en de Smalbladige es slachtoffer van de essentaksterfte, maar er zijn nog zo ontzettend veel andere essen aan te planten in de openbare ruimte die nog totaal onbekend zijn in Nederland. Wij denken nog veel te vaak dat de excelsior alleen op de wereld is, het is een schande! We moeten verder kijken dan onze neus lang is, zodat we kunnen stoppen met al dat gejank over ziekten in (een beperkt deel) van de essen. Auteur: Jan P. Mauritz (VRT) “Zo, geachte lezers van dit feuilleton, weer lekker nog maar tot zijn recht komt in de openhaard. geel in de zomer en in de herfst fantastisch mooi uitgerust terug van de vakantie en met goede “Opstoken die bende!!’ Dan is er ook nog de CV goudgeel. Het is een prima straat en laanboom in moed en heldere geest wederom aan de arbeid, ‘Jaspidea’ die ook de Nederlandse naam Goudes bredere profielen en bij een optimale groeiplaats ik hoop het van harte voor u. De meesten van draagt, een selectie uit Frankrijk(1802) en die ook goed in verhardingen toepasbaar. u zullen bij het lezen van dit deel de vakantie ca. 12 tot 14 meter hoog wordt, een half open al wel achter de rug hebben. Uw schrijver zal breed piramidale kroon vormt waarvan de jonge NB op het moment van verschijnen van deze editie takken geelgroen gestreept zijn, het blad geel Dit voorbeeld, vrienden - en zo zijn er legio - zijn van Boomzorg ergens aan de oostzijde van de uitloopt vervolgens groenachtig wordt en als 3 bomen die allemaal de Nederlandse naam Middellandse Zee vertoeven en daar, naast alle herfstkleur weer prachtig goudgeel wordt. -

Patterns of Flammability Across the Vascular Plant Phylogeny, with Special Emphasis on the Genus Dracophyllum
Lincoln University Digital Thesis Copyright Statement The digital copy of this thesis is protected by the Copyright Act 1994 (New Zealand). This thesis may be consulted by you, provided you comply with the provisions of the Act and the following conditions of use: you will use the copy only for the purposes of research or private study you will recognise the author's right to be identified as the author of the thesis and due acknowledgement will be made to the author where appropriate you will obtain the author's permission before publishing any material from the thesis. Patterns of flammability across the vascular plant phylogeny, with special emphasis on the genus Dracophyllum A thesis submitted in partial fulfilment of the requirements for the Degree of Doctor of philosophy at Lincoln University by Xinglei Cui Lincoln University 2020 Abstract of a thesis submitted in partial fulfilment of the requirements for the Degree of Doctor of philosophy. Abstract Patterns of flammability across the vascular plant phylogeny, with special emphasis on the genus Dracophyllum by Xinglei Cui Fire has been part of the environment for the entire history of terrestrial plants and is a common disturbance agent in many ecosystems across the world. Fire has a significant role in influencing the structure, pattern and function of many ecosystems. Plant flammability, which is the ability of a plant to burn and sustain a flame, is an important driver of fire in terrestrial ecosystems and thus has a fundamental role in ecosystem dynamics and species evolution. However, the factors that have influenced the evolution of flammability remain unclear.